[ad_1]
(noticias nanowerk) Un equipo dirigido por investigadores del SANKEN (Instituto de Investigación Científica e Industrial) de la Universidad de Osaka ha utilizado cristalografía de neutrones para obtener imágenes de todos los átomos en un radical intermedio de una enzima amina oxidasa de cobre. Revelaron detalles previamente desconocidos, como cambios conformacionales precisos, que ayudan a explicar la bioquímica de la enzima. Este trabajo podría ayudar a los investigadores a desarrollar enzimas que permitan una química inusual o que sean muy eficientes a temperatura ambiente y útiles en la industria química.
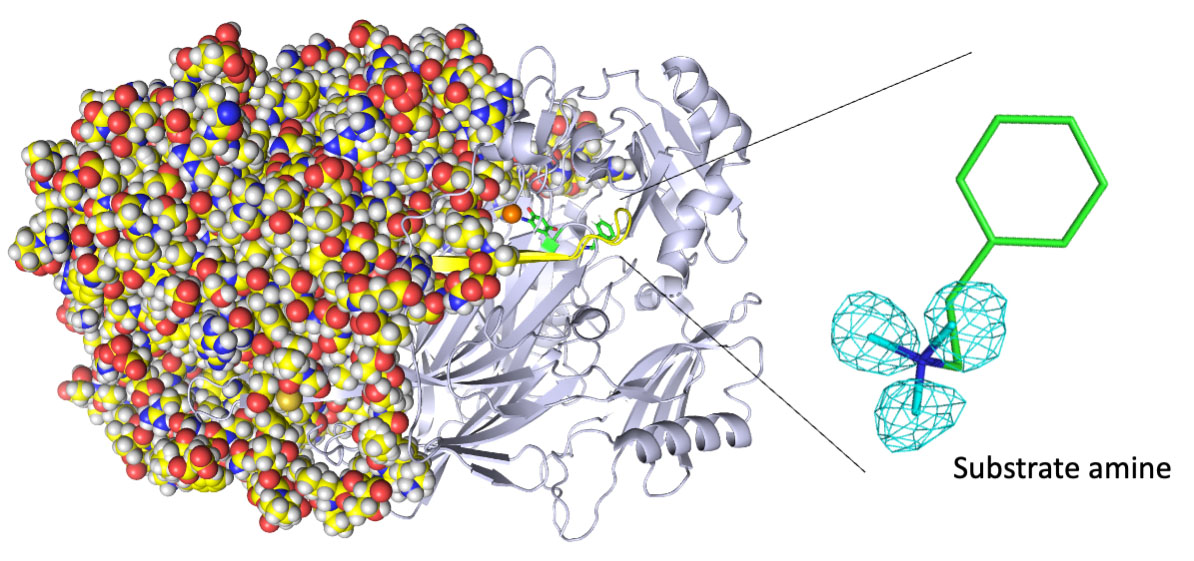
Un equipo dirigido por investigadores de la Universidad de Osaka está utilizando cristalografía de neutrones para mapear todos los átomos en los intermedios de reacción bioquímica de una enzima, lo que podría ayudar a desarrollar enzimas para la industria química.
A medida que sus heridas sanan y su hígado desintoxica una toxina que ingirió, como la histamina, puede agradecer a la clase de enzimas cobre amina oxidasa por su ayuda. Identificar las posiciones precisas de los átomos de hidrógeno más pequeños en estas enzimas es un desafío con las tecnologías actuales, pero es fundamental para el desarrollo de enzimas mejoradas que exhiban una reactividad bioquímica inusual pero útil.
Bueno, en un estudio publicado en catálisis SCA (“La cristalografía de neutrones de un intermedio radical de semiquinona de la aminooxidasa de cobre revela un cambio conformacional asistido por sustrato del cofactor de peptidilquinona”), un equipo dirigido por investigadores de la Universidad Médica y Farmacéutica de Osaka y la Universidad de Osaka utilizó cristalografía de neutrones para obtener imágenes de la estructura atómica de una enzima cobre amino oxidasa Este estudio proporciona una visión estructural sin precedentes de la bioquímica de la enzima.
Algunas enzimas cobre amina oxidasa exhiben una bioquímica inusual, como el túnel cuántico, que permite velocidades de reacción que de otro modo serían inexplicablemente rápidas. Aunque a menudo resulta difícil determinar la posición exacta de cada átomo de hidrógeno en la enzima, este conocimiento es importante para el desarrollo de las correspondientes enzimas artificiales. Los investigadores suelen obtener la estructura átomo por átomo de las enzimas mediante cristalografía de rayos X. Sin embargo, esta técnica obtiene información estructural mediante la difracción de electrones en la enzima. Esto significa que no basta con obtener imágenes de los átomos de hidrógeno, que generalmente sólo contienen un electrón. La cristalografía de neutrones, que analiza la difracción de los núcleos atómicos en la enzima (todos los átomos tienen un núcleo), es una técnica de imagen alternativa que los investigadores eligieron para su trabajo.
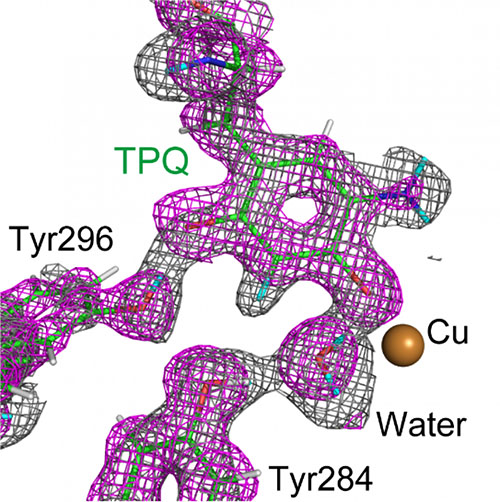
«Hay preguntas sobre la dependencia del pH, el cambio conformacional y la estabilización intermedia radical de nuestra enzima que la cristalografía de rayos X por sí sola no puede explicar completamente», explica Takeshi Murakawa, autor principal del estudio. «La cristalografía de neutrones es muy adecuada para responder a estas preguntas».
Los investigadores obtuvieron numerosos conocimientos. Por ejemplo, mapearon el estado de protonación/desprotonación (en relación con el pH) de sitios dentro de la enzima que son importantes para estabilizar especies radicales (es decir, átomos particularmente reactivos que contienen un electrón desapareado). También caracterizaron los movimientos del cofactor topaquinona de la enzima (deslizamiento, inclinación y semirotación) que facilitan la transferencia de un solo electrón dentro de la enzima.
«Revelamos la unión de una segunda molécula de un sustrato de amina de alta afinidad durante la reacción enzimática, un evento previamente desconocido en el sitio activo de la enzima», dice Toshihide Okajima, autor principal. «La cristalografía de rayos X no detecta estos conocimientos».
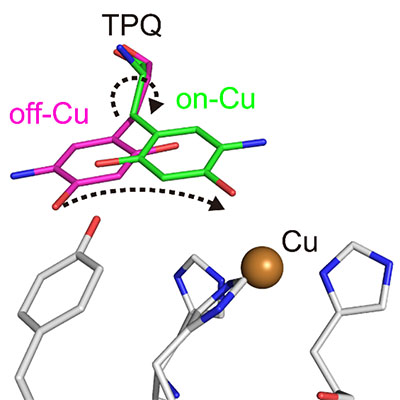
Este trabajo proporcionó detalles estructurales previamente desconocidos de una enzima cobre amina oxidasa que tiene muchas funciones en el metabolismo bioquímico. Revelar la ubicación precisa de los átomos de hidrógeno en la enzima ayuda a explicar su eficiencia a temperaturas y presiones fisiológicas. En el futuro, los investigadores podrían aplicar estos hallazgos para desarrollar enzimas artificiales utilizadas en la industria química.
[ad_2]