[ad_1]
(noticias nanowerk) Las jaulas de proteínas que se encuentran naturalmente en los microbios ayudan a que su contenido resista el duro entorno intracelular, una observación que tiene aplicaciones en muchas aplicaciones biotecnológicas. Los investigadores de Tokyo Tech desarrollaron recientemente un enfoque biotecnológico innovador utilizando bacterias genéticamente modificadas; Estas bacterias pueden construir jaulas de proteínas alrededor de cristales de proteínas. Este método de biosíntesis intracelular genera de manera eficiente complejos proteicos altamente personalizados que podrían encontrar aplicación como catalizadores avanzados de estado sólido y nanomateriales funcionalizados.
Las tesis centrales
Investigación
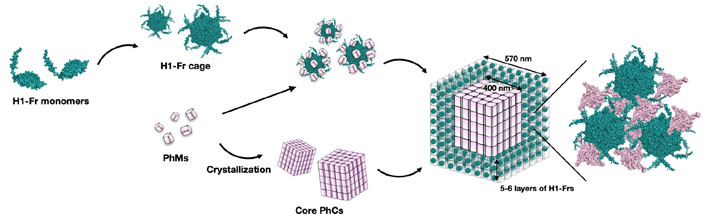
Este diagrama muestra cómo los monómeros H1-Fr y los monómeros de poliedrina (PhM) se combinan para formar espontáneamente una estructura compleja de núcleo-cubierta internamente. E. coli bacterias
En la naturaleza, las proteínas pueden ensamblarse en complejos organizados con innumerables formas y propósitos. Gracias a los notables avances en bioingeniería de las últimas décadas, los científicos ahora pueden crear conjuntos de proteínas personalizados para aplicaciones específicas. Por ejemplo, las jaulas de proteínas pueden encerrar enzimas que actúan como catalizadores para una reacción química objetivo, lo que les permite resistir un entorno celular potencialmente hostil. De manera similar, los cristales de proteínas (estructuras compuestas de unidades proteicas repetidas) pueden servir como andamios para la síntesis de materiales sólidos con extremos funcionales expuestos.
Sin embargo, incorporar (o “encapsular”) proteínas extrañas en la superficie de un cristal de proteína es un desafío. Por lo tanto, ha sido difícil lograr la síntesis de cristales de proteínas que encapsulan conjuntos de proteínas extrañas. Hasta la fecha, no existen métodos eficaces para lograr este objetivo y los tipos de cristales de proteínas producidos son limitados. Pero ¿qué pasaría si las máquinas de células bacterianas pudieran lograr este objetivo?
En un estudio reciente, un equipo de investigación del Instituto de Tecnología de Tokio, incluido el profesor Takafumi Ueno, informó sobre un nuevo método interno de la célula para encapsular jaulas de proteínas con diferentes funciones en cristales de proteínas. Su artículo, publicado en nano letras (“Displaying a Protein Cage on a Protein Crystal by In-Cell Crystal Engineering”) representa un avance significativo en la tecnología de cristales de proteínas.
La estrategia innovadora del equipo implica modificar genéticamente la bacteria Escherichia coli para producir dos componentes básicos: monómero de poliedrina (PhM) y ferritina modificada (Fr). Por un lado, los PhM se combinan de forma natural en las células y forman un cristal de proteína bien estudiado llamado cristal poliédrico (PhC). Por otro lado, se sabe que las unidades de 24 Fr se combinan para formar una jaula de proteínas estable. “La ferritina se utiliza ampliamente como plantilla para construir bionanomateriales modificando sus superficies internas y externas. Por lo tanto, si la formación de una jaula de Fr y su posterior inmovilización en PhC se pueden llevar a cabo simultáneamente en una sola célula, las aplicaciones de «cristales de proteínas intracelulares como materiales biohíbridos se están expandiendo», explica el profesor Ueno.
Para inmovilizar las jaulas de Fr en PhC, los investigadores modificaron el gen que codifica Fr para que contenga una etiqueta de hélice α (H1) de PhM, creando H1-Fr. La razón de este enfoque es que las hélices H1 presentes naturalmente en las moléculas PhM interactúan significativamente con las marcas en H1-Fr y actúan como «agentes de reclutamiento» que unen las proteínas extrañas al cristal.
Utilizando microscopía avanzada, técnicas analíticas y químicas, el equipo de investigación probó la validez del enfoque propuesto. A través de varios experimentos, descubrieron que los cristales resultantes tenían una estructura núcleo-capa, es decir, un núcleo cúbico de PhC de unos 400 nanómetros de ancho, cubierto por cinco o seis capas de jaulas de H1-Fr.
Esta estrategia para la biosíntesis de cristales de proteínas funcionales es prometedora para aplicaciones en medicina, catálisis e ingeniería de biomateriales. «Las jaulas H1-Fr tienen el potencial de inmovilizar moléculas externas en su interior para el transporte molecular», señala el profesor Ueno. “Nuestros resultados sugieren que las estructuras núcleo-cubierta de H1-Fr/PhC, con jaulas de H1-Fr en la superficie exterior, como el núcleo de PhC, pueden controlarse individualmente a nivel de nanoescala. Al acumular varias moléculas funcionales en el núcleo PhC y la jaula H1-Fr, se pueden construir cristales jerárquicos controlados a nanoescala para aplicaciones biotecnológicas avanzadas”.
[ad_2]

