[ad_1]
(noticias nanowerk) Durante décadas, los investigadores han estado buscando formas de manipular e identificar con precisión moléculas individuales, como el ADN, en entornos líquidos. Estas capacidades podrían revolucionar áreas que van desde el diagnóstico de enfermedades hasta el desarrollo de fármacos. Sin embargo, la aleatoriedad de los movimientos moleculares en los líquidos ha obstaculizado el progreso.
Ahora, científicos de la Universidad de Shenzhen y la Universidad China de Hong Kong informan avances prometedores en técnicas de pinzas ópticas que permiten un control excelente sobre partículas biológicas a nanoescala (Luz: ciencia y aplicaciones“Nanopinzas optotérmicas impulsadas por CRISPR: manipulación diversa de bionanopartículas e identificación de nucleótidos individuales”).
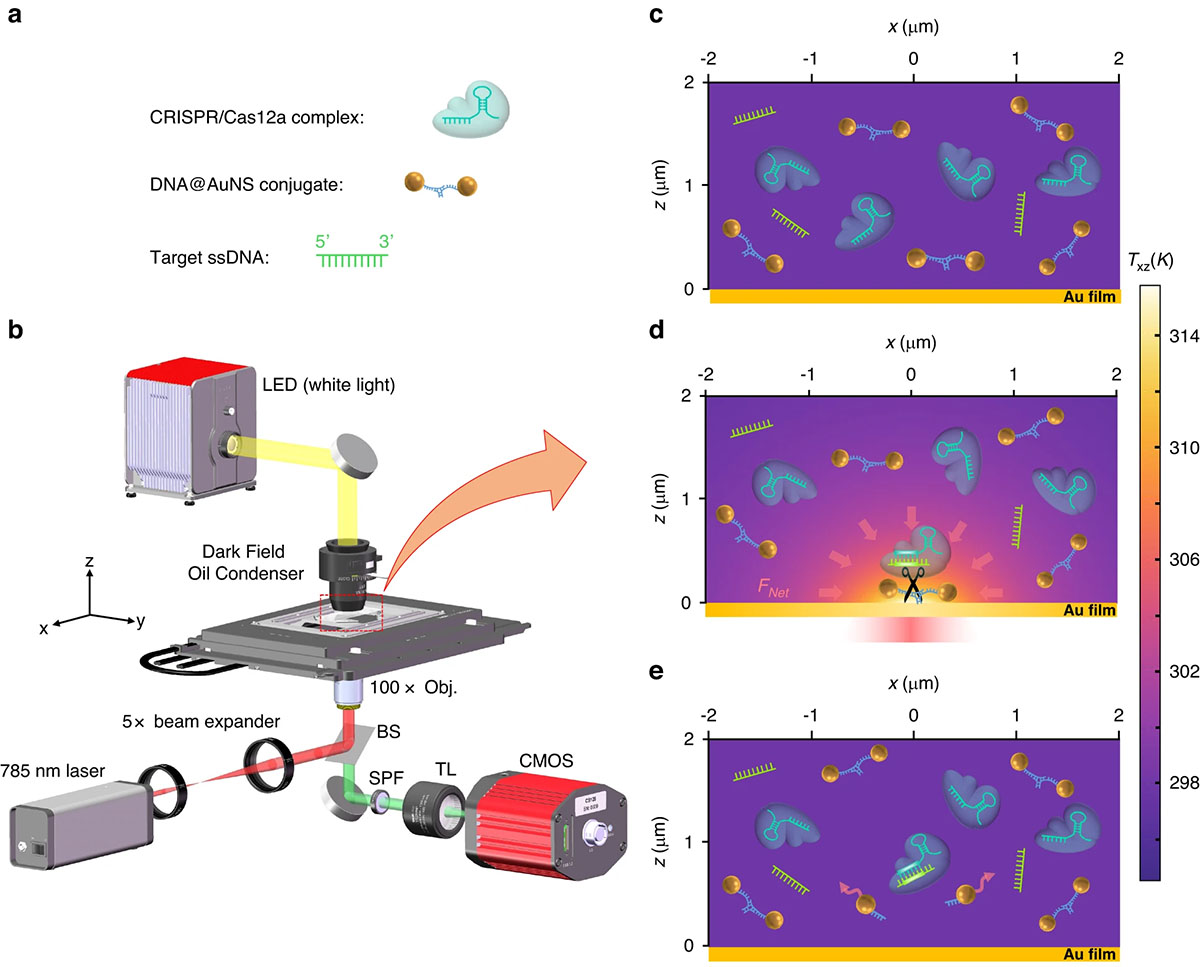
Las trampas ópticas, que utilizan rayos láser para capturar objetos microscópicos, fueron en sí mismas un avance transformador y ganaron el Premio Nobel de Física de 2018. Sin embargo, las pinzas tradicionales tienen limitaciones que las nuevas “nanopinzas optotérmicas impulsadas por CRISPR” (CRONT) pretenden superar: les resulta difícil capturar elementos a nanoescala como el ADN y las proteínas. Y, lo que es más importante, las trampas clásicas no pueden determinar la composición molecular de las partículas atrapadas sin más investigación.
Las innovaciones de CRONT abordan estas limitaciones de dos maneras. En primer lugar, utilizan fuerzas termodinámicas como el calor y los gradientes de concentración para recolectar y manipular biomoléculas. En segundo lugar, integran CRISPR –la reconocida herramienta de corte de ADN que ganó el Premio Nobel en 2020– para identificar secuencias de nucleótidos directamente en la trampa óptica.
Como explica el autor principal, Han Zhang, «diseñamos CRONT para enriquecer las moléculas de ADN objetivo y cumplir con los requisitos térmicos precisos para la escisión mediada por CRISPR, todo dentro de una trampa óptica en el límite de difracción». e identificar biomoléculas individuales”.
Pero ¿por qué manipular moléculas individuales? Los avances en esta área podrían avanzar en la detección rápida de enfermedades o guiar con precisión a CRISPR para editar genes en las células. Además, el control de nanopartículas como el ADN permite estudiar los mecanismos biológicos de cada molécula individual. «Pero es increíblemente difícil», dice Zhang. «La sacudida aleatoria de las moléculas debido al movimiento browniano es proporcionalmente más pronunciada en escalas más pequeñas».
Las primeras trampas ópticas utilizaban el pulso de luz para vencer las fuerzas brownianas. Pero la intensidad del láser requerida a menudo dañaba biomoléculas sensibles. Los métodos posteriores agregaron cosas como plasmónicos y campos eléctricos. Sin embargo, estas pinzas todavía tienen problemas con objetivos biológicos diminutos como el ADN. Además, las trampas ópticas por sí solas no pueden determinar qué molécula se está capturando; la verificación del objetivo requiere sondas secundarias.
CRONT evita estos problemas mediante fuerzas termodinámicas causadas por efectos optotérmicos. Una fina película de oro se calienta cuando se ilumina con un láser infrarrojo. El campo de temperatura generado, a su vez, mueve las moléculas mediante fenómenos naturales como la termoforesis y la difusioforesis. «Analizamos meticulosamente cómo cada componente de fuerza recoge partículas en el punto láser», explica Zhang.
Sorprendentemente, los investigadores demostraron cómo la iluminación variable por sí sola puede agregar varias entidades a nanoescala, como ADN, proteínas y nanopartículas, en las ubicaciones deseadas. Debido a que las fuerzas aumentan con el tamaño de un objeto y la química de la superficie, cada biomolécula exhibió un comportamiento de captura diferente. Y a diferencia de las trampas ópticas tradicionales, CRONT proporcionó suficiente fuerza para capturar y manipular hebras individuales de ADN.
Pero la capacidad más innovadora de CRONT es su detección de objetivos incorporada. El calor local se fijó en 37°C, la temperatura precisa para la escisión del ADN mediada por CRISPR. Al introducir elementos CRISPR en la región de captura, las secuencias capturadas por CRONT pueden interrogarse directamente e incluso cortarse. Las imágenes posteriores de las nanopartículas unidas a ADN separadas confirman la presencia de genes diana.
El en el sitio El enfoque logró una sensibilidad increíble de sólo 25 átomos por microlitro (unas 150 moléculas). Incluso se pudieron detectar pequeños cambios de un solo nucleótido. Según Zhang, «la especificidad permite la detección de mutaciones virales que son críticas para brotes emergentes como el COVID-19». No se requiere amplificación ni etiquetado, lo que permite una evaluación rápida.
CRONT combina de forma única manipulación óptica, reacciones controladas térmicamente y detección basada en CRISPR en una plataforma integrada. Los investigadores anticipan que CRONT podría avanzar en el diagnóstico molecular en el lugar de atención y en las técnicas de edición genómica de próxima generación que están reguladas espacial y temporalmente con resolución unicelular. Aunque CRONT sigue siendo una primera prueba de concepto, demuestra que las técnicas de captura óptica termodinámica pueden abrir posibilidades sin precedentes.
[ad_2]

