[ad_1]
(noticias nanowerk) Durante décadas, los investigadores han buscado un mayor control sobre la distribución y actividad de los fármacos terapéuticos para minimizar los efectos secundarios no deseados y al mismo tiempo maximizar la eficacia. La mayoría de los fármacos aprobados, como las moléculas pequeñas y los anticuerpos monoclonales, actúan de forma sistémica y tienen poca precisión innata sobre dónde se acumulan en el cuerpo y cuánto tiempo persisten. Esta falta de precisión desencadena reacciones tóxicas, desalienta las dosis altas y limita el progreso.
Recientemente, los avances en la nanotecnología del ADN estructural han abierto una forma completamente nueva de ejercer control espacial sobre el comportamiento de los fármacos utilizando nanoestructuras programables y autoensamblables con formas y química definidas. A diferencia de los portadores de fármacos pasivos anteriores, como los liposomas y los polimerosomas, estos sistemas de ADN inteligentes cuentan con programabilidad modular, geometría precisa a nanoescala y restos de superficie fácilmente sintonizables que imparten direccionalidad.
En un nuevo estudio publicado en Informes científicos Los investigadores (“Biodistribution and Function of Coupled Polymer-DNA Origami Nanostructures”) demuestran el poder de acoplar aptámeros dirigidos a enfermedades a nanoestructuras de ADN estabilizadas con polietilenglicol (PEG) para concentrar y mantener la actividad terapéutica dentro de los sitios del tejido objetivo. Los investigadores examinaron varias nanoestructuras en forma de varilla con diferentes tamaños y relaciones de aspecto y descubrieron que las partículas más largas de más de 100 nm persistían mucho más tiempo. en vivo mientras que se difunde más lentamente lejos de los lugares de inyección.
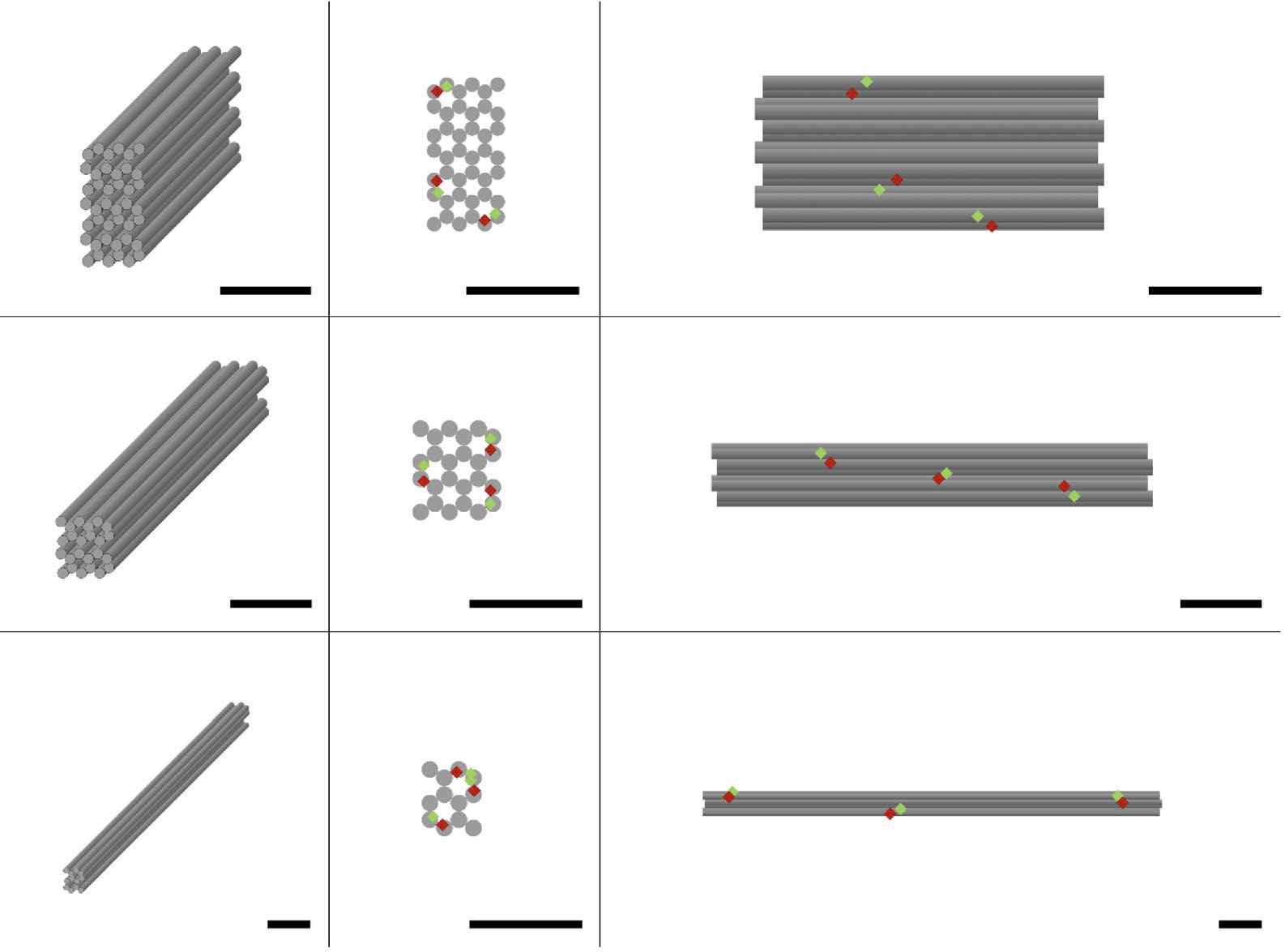
La unión de aptámeros dirigidos a la citocina inflamatoria TNF-alfa produjo efectos antiinflamatorios en modelos murinos de reacción de hipersensibilidad de tipo retardado (DTHR). Los ratones tratados con nanoestructuras de ADN neutralizantes de TNF-alfa mostraron menos inflamación del tejido, menos infiltración de células inmunes y menos engrosamiento epidérmico, comparable a los anticuerpos monoclonales anti-TNF-alfa. Pero a diferencia de los anticuerpos tradicionales, que se distribuyen sistémicamente por todo el cuerpo, las nanoestructuras de aptámero permanecieron concentradas en el tejido objetivo.
Este efecto de localización concentra el efecto terapéutico en los sitios de la enfermedad evitando al mismo tiempo la exposición sistémica, aumentando así la ventana terapéutica. También reduce la dosis necesaria para obtener resultados de tratamiento equivalentes. La modularidad de estas nanoestructuras programables permite aún más la optimización y multiplexación personalizadas mediante un fácil intercambio de fracciones terapéuticas y dirigidas.
Los resultados resaltan el potencial disruptivo de las nanoestructuras de ADN autoensambladas como portadores de fármacos inteligentes con control espacial inherente. A medida que los costos continúan disminuyendo exponencialmente, estos sistemas de ADN de precisión podrían reemplazar las tecnologías convencionales, como los anticuerpos monoclonales, para mejorar la especificidad y, al mismo tiempo, acelerar el desarrollo de cócteles de aptámeros sinérgicos, la administración de fármacos localizada en tejidos y la medicina personalizada adaptada a la genética individual y los fenotipos de enfermedades.
[ad_2]

