[ad_1]
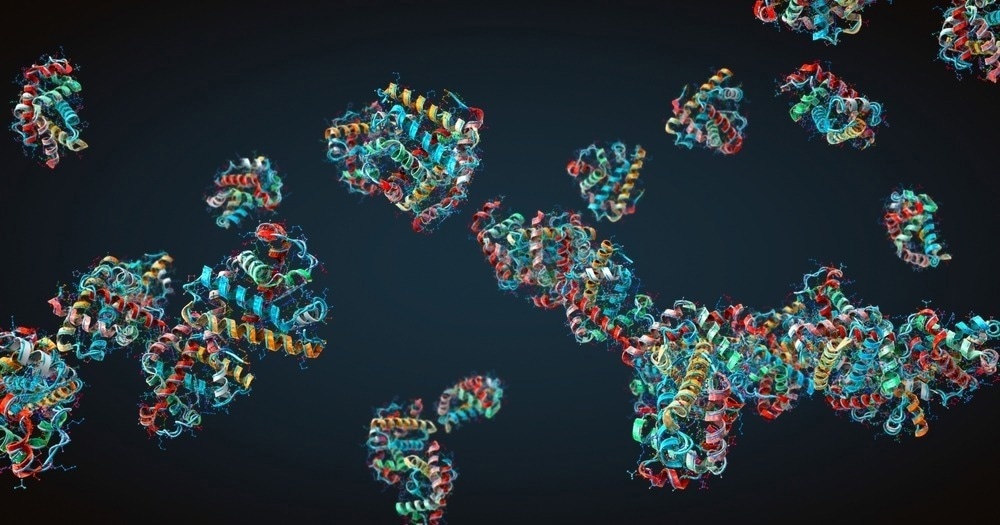
La proteómica y el diagnóstico clínico están siendo transformados por nuevas tecnologías de secuenciación de proteínas con mayor sensibilidad y mayor rendimiento.
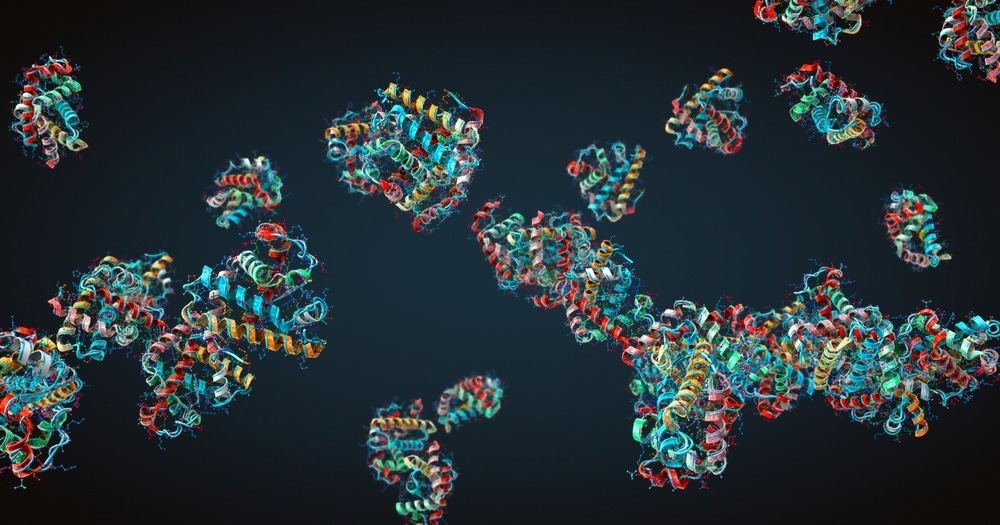
Fuente de la imagen: V/Shutterstock.com
Un equipo de investigación dirigido por el profesor Haichen Wu del Instituto de Química de la Academia China de Ciencias (CAS) y el profesor Lei Liu del Instituto de Física de Altas Energías de la CAS, junto con sus colaboradores, ha desarrollado un nuevo enfoque de secuenciación de péptidos basado en la Detección de nanoporos asistida por interacción huésped-huésped, publicado en Métodos naturales.
La historia de la secuenciación de proteínas se remonta al descubrimiento de Sanger de la secuencia completa de aminoácidos de la insulina en la década de 1950. Actualmente, sólo existen dos técnicas principales disponibles para la secuenciación de proteínas: espectrometría de masas y degradación de Edman.
La detección de nanoporos es el último método “disruptivo” de una sola molécula que ha ganado un impulso significativo en el desarrollo de la secuenciación de ADN de próxima generación en las últimas décadas. Gracias a esta inspiración, los científicos ahora utilizan la secuenciación de proteínas de una sola molécula.
Lograr el transporte unidireccional de cadenas peptídicas cargadas heterogéneamente a través de un nanoporo y la identificación eléctrica de 20 aminoácidos diferentes o sus combinaciones son dos de los formidables obstáculos en la secuenciación de nanoporos de proteínas.
Los investigadores desarrollaron el enfoque de secuenciación alternativo en este estudio basándose en un mejor método de detección de nanoporos respaldado por la interacción huésped-huésped.
Primero, se obtuvo una mezcla de aminoácidos usando carboxipeptidasas para degradar los péptidos modelo. A continuación, fue crucial utilizar un conector covalente para unir los aminoácidos liberados a un FGGCD8⊂CB[7] Sonda peptídica. Luego, el complejo se sometió a ensayos de translocación utilizando α-hemolisina de tipo salvaje o sus mutaciones.
Finalmente, el aminoácido X fue identificado mediante el bloqueo actual de cada FGGC(X)D8⊂CB[7] El péptido y el orden de escisión enzimática o la secuencia peptídica se determinaron por su abundancia relativa.
Este estudio representa una demostración de prueba de concepto de una nueva técnica que puede determinar con precisión la secuencia de aminoácidos de un péptido. Esto representa una mejora significativa y abre una opción viable para el futuro de la secuenciación de proteínas, aunque aún persisten limitaciones importantes.
Referencia de la revista:
Zhang, N., et al. (2023) Secuenciación de péptidos basada en el reconocimiento de nanoporos asistido por la interacción huésped-huésped. Métodos naturales. doi:10.1038/s41592-023-02095-4
Fuente: https://english.cas.cn/
[ad_2]