[ad_1]
(noticias nanowerk) Los péptidos, cadenas cortas de aminoácidos y componentes vitales de las proteínas, están a la vanguardia de la innovación biotecnológica. Estas moléculas biológicas son esenciales para numerosos procesos biológicos como el transporte de oxígeno y electrones.
Inspirándose en la naturaleza, los investigadores son pioneros en el desarrollo de péptidos sintéticos que forman fibras a nanoescala. Estas fibras son particularmente intrigantes porque conducen electricidad cuando se combinan con hemo, una sustancia natural que es crucial para el movimiento de electrones en las proteínas.
Los resultados fueron publicados en Nanoescala (“Diseño de conjuntos anfífilos de péptidos multihemos 1D que recuerdan a los sistemas naturales”).
La investigación investiga cómo la conductividad eléctrica de estas nanofibras peptídicas se ve influenciada por la longitud y la composición específica de la secuencia de aminoácidos. Comprender estos parámetros estructurales es crucial porque determinan la función de los péptidos en la naturaleza y su potencial en biotecnología. Estos incluyen la longitud de la secuencia de los segmentos peptídicos y la disposición de aminoácidos específicos dentro de un péptido.
Los resultados del estudio son cruciales para el desarrollo de conjuntos de péptidos que puedan formar fibras a nanoescala capaces de transportar electrones a largas distancias. Estos avances son prometedores para aplicaciones en dispositivos médicos, biosensores, robótica y el desarrollo de nuevas enzimas para industrias que van desde la atención sanitaria hasta la limpieza del hogar.
Al explorar los campos de la ciencia de materiales y la bioquímica, los investigadores están particularmente interesados en las nanoestructuras de proteínas y péptidos naturales, conocidas por su potencial como materiales bioelectrónicos. La creación de análogos sintéticos capaces de formar nanoestructuras unidimensionales es un paso importante hacia la comprensión de los sistemas naturales y el desarrollo de nuevos materiales.
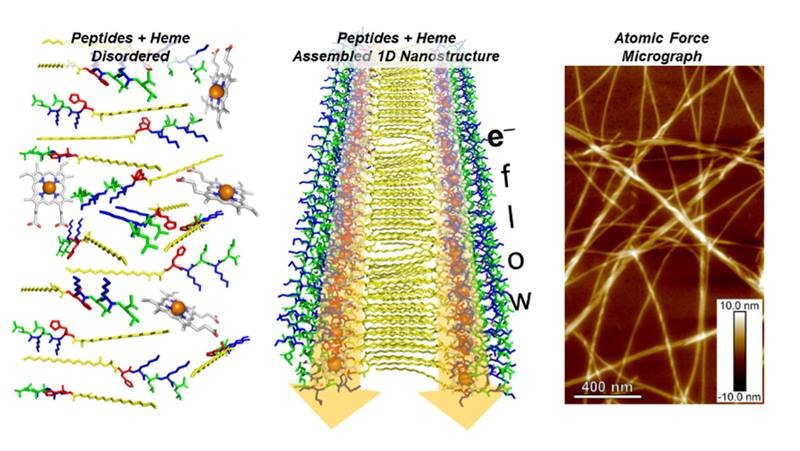
En el Centro de Materiales a Nanoescala del Laboratorio Nacional Argonne se ha estudiado una serie de péptidos, PA-(Kx)n o PA-Kxn. Estos péptidos se autoensamblan en nanoestructuras en capas unidimensionales. Cada péptido consta de alanina modificada (c16-A), histidina (H), lisina (K) y un aminoácido hidrofóbico como leucina (L), isoleucina (I) o fenilalanina (F) con diferentes longitudes de repetición de secuencia.
El equipo de investigación se centró en cómo la longitud de la secuencia peptídica y la identidad del aminoácido hidrófobo afectan factores cruciales como la afinidad de unión del hemo a los péptidos preensamblados, la densidad del hemo y las propiedades electrónicas. Descubrieron que una secuencia de dos longitudes daba la mayor afinidad de unión, lo que llevó a ensamblajes a nanoescala que organizaban el hemo en matrices ordenadas. Estas nanofibras, con la excepción de PA-KL1, exhibieron una relación de aspecto larga independientemente de la longitud y secuencia de las unidades repetidas.
Este descubrimiento destaca el potencial de estructuras como los materiales bioelectrónicos supramoleculares, que podrían revolucionar la detección biomédica y el desarrollo de materiales enzimáticos.
[ad_2]

