[ad_1]
(noticias nanowerk) Algunas vacunas Covid-19 utilizaron de forma segura y eficaz nanopartículas lipídicas (LNP) para entregar ARN mensajero a las células. Un nuevo estudio del MIT muestra que varias nanopartículas podrían usarse para una posible terapia para la enfermedad de Alzheimer (EA). En pruebas en varios modelos de ratón y con células humanas cultivadas, una formulación LNP recientemente adaptada entregó eficazmente pequeños ARN de interferencia (ARNip) a las células inmunes microgliales del cerebro para suprimir la expresión de una proteína relacionada con la inflamación excesiva en la enfermedad de Alzheimer.
Las tesis centrales
Un nuevo estudio sugiere que las nanopartículas lipídicas (LNP) podrían administrar eficazmente terapias de ARN a la microglía del cerebro y potencialmente tratar la enfermedad de Alzheimer.
Se descubrió que la formulación personalizada de LNP suprime una proteína relacionada con la inflamación del Alzheimer y mostró resultados prometedores en modelos de ratón y cultivos de células humanas.
A diferencia de los métodos existentes, el diseño LNP exclusivo del estudio demostró una alta eficiencia de entrega y seguridad al apuntar a la microglía en el cerebro sin afectar otros órganos.
Este enfoque representa un avance significativo en la tecnología de administración de ARN y revela nuevas vías potenciales para el tratamiento de enfermedades neuroinflamatorias.
Se necesita más investigación para traducir estos hallazgos en ensayos en humanos, pero los resultados ofrecen una prueba de principio prometedora para terapias futuras.
Investigación
En un estudio anterior (Revista de medicina experimental«Una nueva clase de moléculas que recluta complejos HDAC/MECP2 en motivos PU.1 reduce la neuroinflamación»), los investigadores demostraron que bloquear las consecuencias de la actividad de la proteína PU.1 ayuda a reducir la neuroinflamación asociada con la enfermedad de Alzheimer y reduce la patología. Los nuevos resultados, publicados en la revista Materiales avanzados (“Nanoparticle-mediated Delivery of Anti-PU.1 Sirna via Localized Intracisterternal Administration Reduces Neuroinflammation”) logra una reducción de la inflamación al suprimir directamente la expresión del gen Spi1, que codifica PU.1. En general, el nuevo estudio también muestra una nueva forma de entregar ARN a la microglía, a la que antes era difícil llegar.
La coautora del estudio, Li-Huei Tsai, profesora Picower de Neurociencia y directora del Instituto Picower para el Aprendizaje, la Memoria y la Iniciativa Cerebral Envejecido, dijo que planteó la hipótesis de que las LNP podrían servir como una forma de administrar ARNip a la microglía porque las células están eliminando los productos de desecho. en el cerebro tienen una fuerte tendencia a absorber moléculas de lípidos. Habló de esto con Robert Langer, profesor del Instituto David Koch, ampliamente conocido por su trabajo pionero en la administración de fármacos con nanopartículas. Decidieron probar la idea de reducir la expresión de PU.1 con un ARNip administrado por LNP.
«Todavía recuerdo el día que solicité una reunión con Bob para discutir la idea de probar las LNP como una carga útil para atacar la microglía inflamatoria», dijo Tsai, miembro de la facultad del Departamento de Ciencias Cognitivas y del Cerebro. «Estoy muy agradecido a la Fundación JPB, que apoyó esta idea sin pruebas preliminares».
El estudiante graduado de Langer Lab, Jason Andresen, y el ex becario postdoctoral de Tsai Lab, William Ralvenius, dirigieron el trabajo y son coautores principales del estudio. Owen Fenton, ex becario postdoctoral en el Laboratorio Langer y ahora profesor asistente en la Facultad de Farmacia Eshelman de la Universidad de Carolina del Norte, es coautor correspondiente junto con Tsai y Langer. Langer es profesor de ingeniería química y bioingeniería en el Instituto Koch para la investigación integral del cáncer.
Perfeccionando una partícula
La forma más sencilla de probar si el ARNip podría suprimir terapéuticamente la expresión de PU.1 habría sido utilizar un dispositivo de administración ya disponible, pero uno de los primeros descubrimientos del estudio es que ninguno de los ocho reactivos disponibles comercialmente hizo que los cultivos fueran seguros y eficaces. para transfectar células similares a la microglía humana en el laboratorio.
En cambio, el equipo tuvo que optimizar un LNP para realizar esta tarea. Los LNP constan de cuatro componentes principales. Al cambiar la estructura de dos de ellos y variar la proporción de lípidos a ARN, los investigadores pudieron desarrollar siete formulaciones para probar. Es importante destacar que sus pruebas implicaron probar sus formulaciones en microglía cultivada, a la que habían inducido a un estado inflamatorio. Al fin y al cabo, esta condición es aquella en la que es necesario el tratamiento propuesto.
Entre los siete candidatos, el equipo denominado «MG-LNP» destacó por su eficiencia de entrega particularmente alta y la seguridad de una carga de ARN de prueba.
Lo que funciona en un plato a veces no funciona en un organismo vivo. Entonces, el equipo probó a continuación la eficacia y seguridad de sus formulaciones de LNP en ratones. Probaron dos métodos de inyección diferentes, en el cuerpo o en el líquido cefalorraquídeo (LCR), y descubrieron que la inyección en el LCR garantizaba una eficacia mucho mayor para atacar la microglía sin afectar las células de otros órganos. Entre las siete formulaciones, se descubrió nuevamente que MG-LNP era la más eficaz para transfectar la microglía. Langer dijo que cree que algún día esto podría abrir nuevas formas de tratar ciertas enfermedades cerebrales con nanopartículas.
Una terapia dirigida
Sabiendo que MG-LNP podría administrar una carga de prueba de microglia tanto en cultivos de células humanas como en ratones, los científicos probaron si el uso de MG-LNP para administrar un ARNip supresor de PU.1 podría reducir la inflamación en la microglia. En los cultivos celulares, una dosis relativamente baja resultó en una reducción del 42 por ciento en la expresión de PU.1 (lo cual es bueno, ya que la microglía requiere al menos algo de PU.1 para vivir). De hecho, la transfección con MG-LNP no provocó ningún daño a las células. También redujo significativamente la transcripción de los genes que aumentan la expresión de PU.1 en la microglía, lo que sugiere que puede reducir múltiples marcadores inflamatorios.
En todas estas y otras medidas, MG-LNP superó a un reactivo disponible comercialmente llamado RNAiMAX que los científicos probaron en paralelo.
«Estos resultados respaldan el uso de la administración de ARNip anti-PU.1 mediada por MG-LNP como una terapia potencial para enfermedades neuroinflamatorias», escribieron los investigadores.
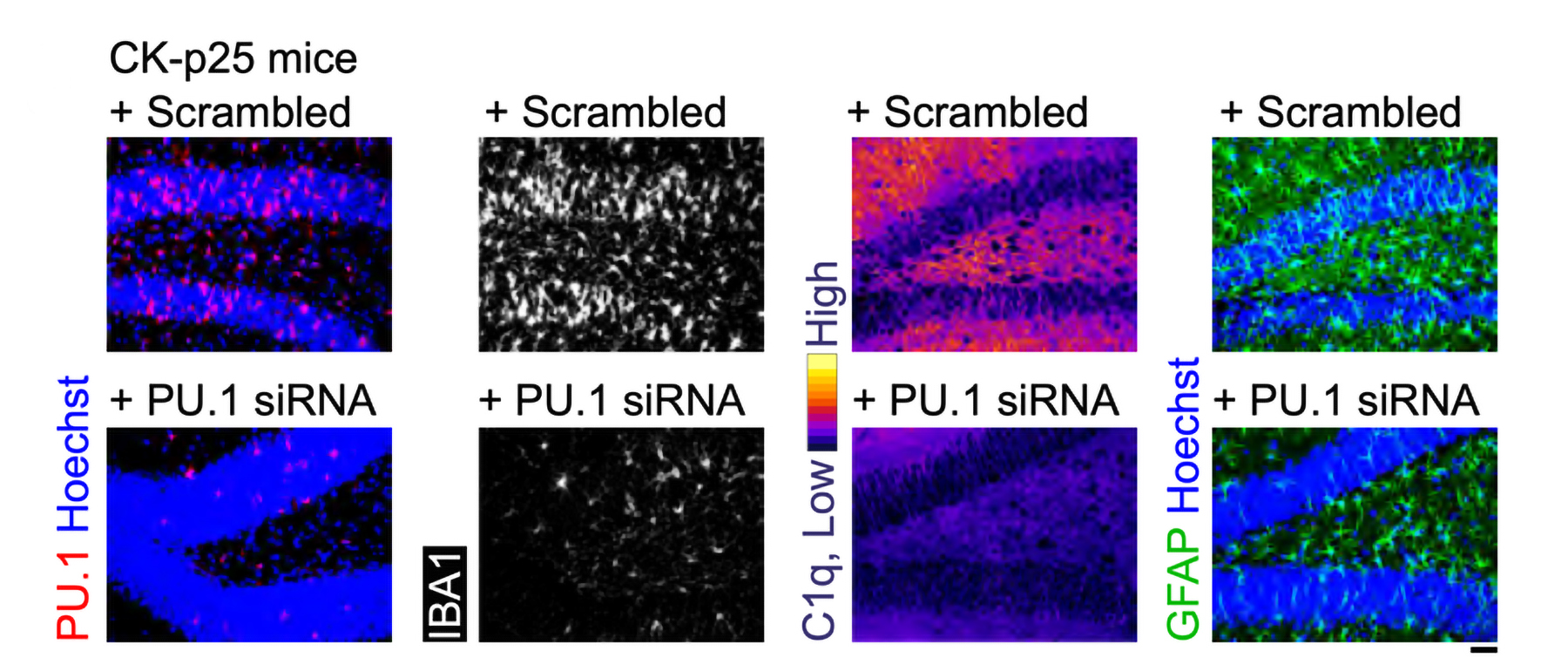
La serie final de pruebas evaluó el desempeño de MG-LNP en la administración del ARNip en dos modelos de inflamación cerebral en ratones. En un caso, los ratones fueron expuestos a LPS, una molécula que simula una infección y estimula una respuesta inflamatoria sistémica. En el otro modelo, los ratones muestran neurodegeneración e inflamación graves cuando una enzima llamada CDK5 es hiperactivada por una proteína llamada p25.
En ambos modelos, la inyección de MG-LNP que portan el ARNip anti-PU.1 redujo la expresión de PU.1 y de marcadores inflamatorios, similares a los de las células humanas cultivadas.
«La administración MG-LNP de ARNip anti-PU.1 puede usarse potencialmente como un tratamiento antiinflamatorio en ratones con inflamación sistémica y en el modelo de ratón CK-p25 de neuroinflamación similar a la EA», concluyeron los científicos, calificando los resultados como una “Prueba de principio”. Se necesitan más pruebas antes de que la idea pueda probarse en pacientes humanos.
[ad_2]

