[ad_1]
(noticias nanowerk) Las vacunas terapéuticas contra el cáncer son una forma de inmunoterapia que no sólo podría destruir las células cancerosas en los pacientes, sino también evitar que el cáncer reaparezca y se propague. Se están estudiando varias vacunas terapéuticas contra el cáncer en ensayos clínicos, pero a pesar de lo prometedoras, los oncólogos clínicos todavía no las utilizan de forma rutinaria para tratar a sus pacientes.
El componente central de las vacunas terapéuticas contra el cáncer son los antígenos que son producidos preferentemente o producidos recientemente por células tumorales (neoantígenos) y permiten que el sistema inmunológico del paciente busque y destruya las células cancerosas. En la mayoría de los casos, estos antígenos no pueden funcionar solos y requieren la ayuda de moléculas adyuvantes que desencadenan una señal de alarma general en las células inmunitarias llamadas células presentadoras de antígenos (APC). Las APC internalizan tanto el antígeno como las moléculas adyuvantes y presentan los antígenos a diferentes tipos de células T. Luego, estas células T lanzan un ataque inmediato contra el tumor o retienen una memoria más duradera del tumor para futuras defensas.
La eficacia de una vacuna contra el cáncer depende de la fuerza y la duración de la “alarma” que sus adyuvantes pueden desencadenar en las APC. Anteriormente, los investigadores descubrieron que la administración simultánea de moléculas de adyuvante y antígeno a las APC utilizando nanoestructuras como el origami de ADN puede aumentar la activación de las APC. Sin embargo, ninguno de estos enfoques examinó sistemáticamente cómo el número y la disposición a nanoescala de las moléculas adyuvantes afectan la inmunidad dirigida a los tumores.
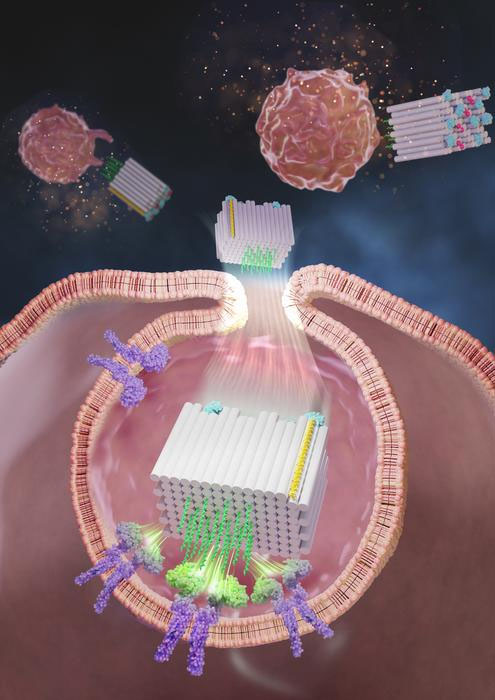
Ahora, un equipo de investigación del Instituto Wyss de la Universidad de Harvard, el Instituto del Cáncer Dana-Farber (DFCI), la Facultad de Medicina de Harvard (HMS) y el Instituto Coreano de Ciencia y Tecnología (KIST) ha desarrollado una plataforma de origami de ADN llamada DoriVac, cuyo núcleo es el componente Es una nanoestructura autoensamblable en forma de bloque cuadrado. Se puede unir un número definido de moléculas adyuvantes a un lado del bloque cuadrado en patrones nanoprecisos y altamente sintonizables, mientras que el lado opuesto puede unirse a antígenos tumorales.
El estudio encontró que las moléculas de un adyuvante llamado CpG, separadas exactamente por 3,5 nanómetros, daban como resultado la estimulación más beneficiosa de las APC, lo que inducía un perfil altamente deseable de células T, incluidas aquellas que matan las células cancerosas (células T citotóxicas). . los que provocan inflamación beneficiosa (células T polarizadas Th-1) y los que proporcionan memoria inmune a largo plazo del tumor (células T de memoria).
Las vacunas DoriVac permitieron a los ratones con tumores controlar mejor el crecimiento del tumor y sobrevivir significativamente más tiempo que los ratones de control. Es importante destacar que la acción de DoriVac también interactúa con la acción de los inhibidores de puntos de control inmunológico, que son una inmunoterapia de gran éxito que ya se utiliza ampliamente en la clínica.
Los resultados se publicarán en Nanotecnología de la naturaleza (“Ajuste de la distribución espacial de CpG con origami de ADN para mejorar la vacunación contra el cáncer”).
«La tecnología de vacuna de origami de ADN de DoriVac combina diversas capacidades de nanotecnología que hemos desarrollado a lo largo de los años con un conocimiento cada vez más profundo de los procesos inmunológicos supresores del cáncer», dijo William Shih, Ph.D., miembro de la Facultad Wyss Core y líder de los equipos del Instituto Wyss. junto con el primer autor Yang (Claire) Zeng, MD, Ph.D. «Prevemos que en el futuro, los antígenos identificados en pacientes con diversos tipos de tumores podrían cargarse rápidamente en origami de ADN prediseñados que contengan adyuvantes para permitir vacunas contra el cáncer personalizadas y de alta eficiencia utilizadas en terapias combinadas con inhibidores de puntos de control aprobados por la FDA». Shih también es profesor en la División de Biología del Cáncer en HMS y DFCI y, como algunos de los otros autores, miembro del Centro multiinstitucional de Inmunoingeniería para Mejorar la Inmunoterapia (i3) en Wyss, financiado por los NIH.
Razonamiento del origami de ADN
El adyuvante CpG es una cadena de ADN sintética compuesta de motivos repetidos de nucleótidos CpG que imitan el material genético de patógenos bacterianos y virales que invaden las células inmunitarias. Al igual que sus homólogos naturales, los adyuvantes CpG se unen a un «receptor de peligro» llamado TLR9 en las células inmunitarias, que a su vez induce una respuesta inmunitaria inflamatoria (innata) que interactúa con la respuesta inmunitaria (adaptativa) inducida por antígenos.
“Sabíamos por trabajos anteriores que los receptores TLR9 deben dimerizarse y agregarse en complejos multiméricos que se unen a múltiples moléculas CpG para desencadenar fuertes respuestas inflamatorias. «Las distancias a nanoescala entre los dominios de unión de CpG en ensamblajes efectivos de TLR9 revelados por el análisis estructural estaban exactamente en el rango de lo que supusimos que podría reflejarse en estructuras de origami de ADN que representan moléculas de CpG espaciadas con precisión», dijo Zeng, profesor de medicina en el momento del estudio y ahora científico senior en DFCI y la Escuela de Medicina de Harvard (HMS). Además de Shih, a Zeng también se unieron en el proyecto los autores principales Ju Hee Ryu, Ph.D., investigador principal de KIST, y David Mooney, Ph.D., miembro de Wyss Founding Core Faculty, quien también es profesor de la Escuela de Ingeniería y Ciencias Aplicadas John A. Paulson de Harvard (SEAS) y uno de los investigadores principales del Centro i3.
Zeng y el equipo crearon vacunas DoriVac con números variables de hebras CpG espaciadas a 2,5, 3,5, 5 o 7 nanómetros en un lado del bloque cuadrado y un antígeno modelo en el lado opuesto era apropiado. Protegieron sus estructuras de la degradación en el cuerpo utilizando un método de modificación química que el grupo de Shih había desarrollado previamente. Cuando fueron internalizadas por varios tipos de APC, incluidas las células dendríticas (DC), que orquestan las respuestas de las células T impulsadas por tumores, las vacunas DoriVac mejoraron la absorción de antígenos en comparación con los controles que consisten en moléculas de antígenos libres. Un espaciamiento de CpG de 3,5 nanómetros produjo las respuestas más fuertes y beneficiosas en las APC, superando significativamente a una vacuna de control que contenía solo moléculas de CpG libres.
«Nos entusiasmó descubrir que la vacuna DoriVac induce preferentemente un estado de activación inmunitaria que respalda la inmunidad antitumoral, lo que los investigadores generalmente esperan de una buena vacuna», dijo Zeng.
Además de la distancia, también influyó la cantidad de moléculas CpG en las vacunas DoriVac. El equipo probó vacunas que contenían entre 12 y 63 moléculas CpG distribuidas de manera óptima y descubrió que 18 moléculas CpG proporcionaban la mejor activación de APC. Esto significó que su enfoque también puede ayudar a limitar la dosis de moléculas CpG, minimizando así los efectos secundarios tóxicos comúnmente observados con los adyuvantes.
Obtenido en traducción (tumoral)
Es importante destacar que estas tendencias in vitro se trasladaron a modelos de tumores de ratón in vivo. Cuando se inyectaron de forma profiláctica debajo de la piel de los ratones, las vacunas DoriVac se acumularon en los ganglios linfáticos más cercanos, donde estimularon las CD. Una vacuna cargada con un antígeno de melanoma impidió el crecimiento de células de melanoma agresivas inyectadas posteriormente. Si bien todos los animales de control habían sucumbido al cáncer el día 42 del experimento, todos los animales protegidos con DoriVac estaban vivos. Las vacunas DoriVac también inhibieron el crecimiento tumoral en ratones donde la formación de tumores de melanoma ya estaba en marcha, con una separación de 18 moléculas CpG a 3,5 nanómetros de distancia produciendo nuevamente efectos máximos sobre las células DC y T y la mayor reducción del crecimiento tumoral.
A continuación, el equipo preguntó si las vacunas DoriVac también podrían mejorar las respuestas inmunitarias causadas por pequeños «neoantígenos» que se encuentran en los tumores de melanoma. Los neoantígenos son objetivos ideales porque son producidos exclusivamente por células tumorales. Sin embargo, a menudo no son muy inmunogénicos, lo que hace que los adyuvantes altamente eficaces sean un componente importante de las vacunas neoantígenas. Una vacuna DoriVac personalizada con cuatro neoantígenos permitió a los investigadores suprimir significativamente el crecimiento tumoral en ratones que produjeron los neoantígenos.
Finalmente, los investigadores preguntaron si DoriVac podría tener sinergia con la terapia de puntos de control inmunológico, que reactiva las células T que han sido silenciadas en los tumores. En ratones, la combinación de ambas terapias condujo a una regresión completa de los tumores de melanoma y evitó que volvieran a crecer cuando los animales fueron expuestos nuevamente a las mismas células tumorales cuatro meses después. Los animales habían desarrollado una memoria inmune del tumor. El equipo logró una eficacia de vacunación similar en un modelo de linfoma en ratón.
«Creemos que el valor de DoriVac para identificar un punto óptimo en la administración de adyuvantes y mejorar la administración y el efecto de los antígenos acoplados puede allanar el camino hacia vacunas clínicas contra el cáncer más efectivas para su uso en pacientes con una variedad de tipos de cáncer», dijo Zeng. Actualmente, el equipo está trasladando la plataforma DoriVac a su aplicación clínica, respaldada por la evaluación del estudio de la distribución de la vacuna y los anticuerpos dirigidos a la vacuna en ratones, así como las citocinas producidas por las células inmunitarias en respuesta a las vacunas in vivo.
«La plataforma DoriVac es nuestro primer ejemplo de cómo nuestra búsqueda de lo que llamamos robótica molecular (moléculas sintéticas bioinspiradas con forma y función programables) puede conducir a terapias completamente nuevas y poderosas». Vacunas de diseño con propiedades adaptadas a desafíos clínicos específicos. Esperamos que se traduzca rápidamente en la clínica”, dijo el director fundador del Instituto Wyss, Donald Ingber, MD, Ph.D., quien también es profesor Judah Folkman de biología vascular en HMS y el Boston Children’s Hospital y profesor de bioinspiración Hansjörg Wyss. Ingeniería en SEAS.
[ad_2]

