[ad_1]
(Noticias de Nanowerk) Cuando piensas en proteínas, las enzimas, las moléculas de señalización y los componentes estructurales de todos los seres vivos, puedes pensar en cadenas individuales de aminoácidos dispuestas como cuentas en un hilo. Pero casi todas las proteínas están formadas por múltiples hebras que se pliegan y unen entre sí, formando superestructuras 3D intrincadas llamadas ensamblajes moleculares. Uno de los pasos más importantes para comprender la biología es descubrir cómo una proteína hace su trabajo, lo que requiere el conocimiento de sus estructuras hasta el nivel atómico.
Durante el siglo pasado, los científicos han desarrollado y utilizado tecnologías sorprendentes como la cristalografía de rayos X y la criomicroscopía electrónica para determinar la estructura de las proteínas, respondiendo así a innumerables preguntas importantes. Pero un nuevo trabajo muestra que comprender la estructura de las proteínas a veces puede ser más complicado de lo que pensamos.
Un grupo de investigadores del Laboratorio Nacional Lawrence Berkeley (Berkeley Lab) estudió la proteína más abundante del mundo, una enzima involucrada en la fotosíntesis llamada Rubisco, y mostró cómo la evolución puede conducir a una sorprendente variedad de arreglos moleculares que realizan la misma tarea. Los resultados, publicados en avances científicos («Structural Plasticity Enables Evolution and Innovation of RuBisCO Assemblies») plantea la posibilidad de que muchas de las proteínas que creíamos conocer realmente existen en otras formas desconocidas.
Por ejemplo, en el pasado, si los científicos resolvían una estructura y encontraban que una proteína era dimérica (que constaba de dos unidades), podían suponer que también existían proteínas similares en forma dimérica. Pero el pequeño tamaño de la muestra y el sesgo de la muestra, factores inevitables ya que es muy difícil convertir las proteínas líquidas de forma natural en formas sólidas y cristalizadas que se pueden estudiar mediante cristalografía de rayos X, oscurecieron la realidad.
«Es como si sales y ves a alguien paseando a su perro, si nunca has visto un perro y luego ves un perro salchicha, dirías, ‘bien, así son todos los perros'». Pero lo que tienes que hacer es ir al parque para perros y ver toda la variedad de perros que hay allí”, dijo el autor principal Patrick Shih, científico de la facultad de ciencias de la vida y director de diseño de biosistemas de plantas en el Joint BioEnergy Institute (JBEI). . «Una conclusión de este artículo que va más allá de Rubisco, a todas las proteínas, es si estamos viendo o no la verdadera diversidad de estructuras en la naturaleza, o si estas distorsiones hacen que parezca que todo parece una salchicha».
Con la esperanza de explorar todos los diferentes arreglos de Rubisco en el parque para perros metafórico y de dónde procedían, el laboratorio de Shih trabajó con expertos en biología estructural del Área de Biociencia, que utilizaron la fuente de luz avanzada de Berkeley Lab. Juntos, el equipo estudió una especie de Rubisco (Forma II) que se encuentra en bacterias y un subconjunto de microbios fotosintéticos, utilizando cristalografía tradicional, una técnica que permite la resolución a nivel atómico, en combinación con otra técnica de solución de estructura, X de ángulo pequeño. dispersión de rayos (SAXS), que tiene una resolución más baja pero puede tomar instantáneas de proteínas en su forma nativa cuando están en mezclas líquidas.
SAXS tiene el beneficio adicional de la capacidad de alto rendimiento, lo que significa que puede procesar docenas de matrices de proteínas individuales en rápida sucesión.
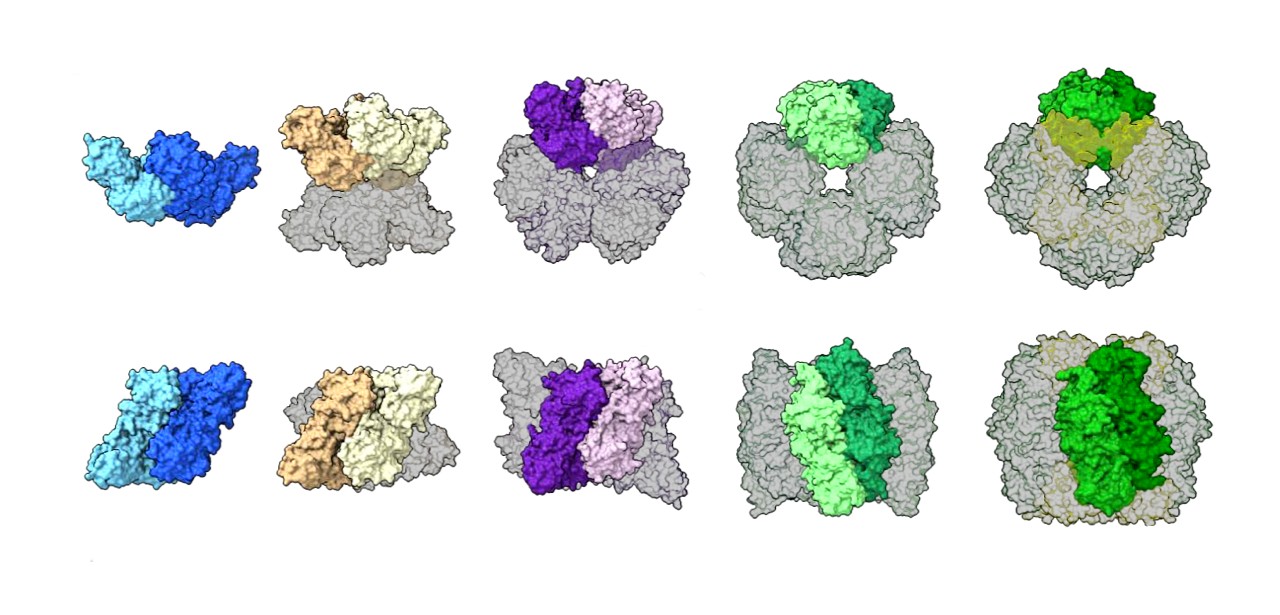
Trabajos anteriores habían demostrado que la especie mejor estudiada de Rubisco en las plantas (Forma I) siempre tiene una disposición de «octámero nuclear» de ocho unidades de proteína grandes dispuestas con ocho unidades pequeñas, mientras que se pensaba que la Forma II existía principalmente como un dímero con un existen algunos ejemplos raros de hexámeros de seis unidades. Después de usar estas técnicas complementarias para estudiar muestras de Rubisco de una variedad de especies microbianas, los autores determinaron que la mayoría de las proteínas de la Forma II de Rubisco son, de hecho, hexámeros con dímeros ocasionales, y descubrieron un ensamblaje de tetrámero (cuatro unidades) nunca antes visto.
La combinación de estos datos estructurales con las respectivas secuencias de genes que codifican proteínas permitió al equipo realizar una reconstrucción de secuencias ancestrales, un método de evolución molecular computacional que puede estimar cómo las proteínas ancestrales se basan en la secuencia y apariencia de las proteínas modernas que evolucionaron a partir de ellas.
La reconstrucción sugiere que el gen de la Forma II Rubisco cambió a lo largo de su historia evolutiva para producir proteínas con una variedad de estructuras que se transforman fácilmente en nuevas formas o vuelven a estructuras más antiguas.
Por el contrario, a lo largo de la evolución, la presión selectiva condujo a una serie de cambios que fijaron la Forma I rubisco, un proceso llamado atrincheramiento estructural, razón por la cual el arreglo octamérico es el único arreglo que vemos hoy. Según los autores, se planteó la hipótesis de que la mayoría de los ensamblajes de proteínas se solidificaron con el tiempo a través de la presión selectiva para refinar su función, como vemos en la Forma I Rubisco. Pero esta investigación sugiere que la evolución también puede favorecer a las proteínas flexibles.
«La gran conclusión de este trabajo es que hay mucha plasticidad estructural», dijo Shih, quien también es profesor asistente en UC Berkeley. «Las proteínas pueden ser mucho más flexibles en todo el campo de lo que pensábamos anteriormente».
Después de completar la reconstrucción de la secuencia ancestral, el equipo realizó experimentos mutacionales para ver cómo cambiar la disposición de Rubisco, en este caso romper un hexámero en un dímero, afectaba la actividad de la enzima. Inesperadamente, esta mutación inducida resultó en una forma de Rubisco que puede utilizar mejor su molécula objetivo, CO2.
Todos los Rubisco naturales comúnmente se unen al O de tamaño similar2 La molécula se aleatoriza, reduciendo la productividad de la enzima. Existe un interés considerable en la ingeniería genética del Rubisco en especies de plantas agrícolas para aumentar la afinidad de la proteína por el CO.2producir cultivos más productivos y eficientes en el uso de los recursos. Sin embargo, se ha puesto mucho énfasis en el sitio activo de la proteína, la región de la proteína donde el CO2 oo2 Corbata.
«Para nosotros, esta es una idea interesante, ya que sugiere que para obtener resultados más fructíferos en la ingeniería de Rubisco, no podemos simplemente mirar la respuesta más simple, es decir, la región de la enzima que realmente interactúa con el CO2», dijo el primer autor Albert Liu, un estudiante de posgrado en el laboratorio de Shih. «Tal vez hay mutaciones fuera de este sitio activo que realmente están involucradas en esta actividad y pueden potencialmente alterar la función de la proteína de la manera que queremos». Así que esto es algo que realmente abre las puertas a futuras vías de investigación”.
El coautor Paul Adams, gerente de laboratorio asociado para ciencias de la vida y vicepresidente de tecnología en JBEI, agregó: “La combinación de técnicas empleadas y la naturaleza interdisciplinaria del equipo fueron una clave real para el éxito. El trabajo subraya el poder de combinar datos genómicos y métodos de biología estructural para investigar uno de los problemas más importantes de la biología y llegar a conclusiones inesperadas”.
[ad_2]

