[ad_1]
(Proyector de Nanowerk) La proteína corona juega un papel crucial no solo en la entrega clínica de nanomateriales, sino también en una variedad de otras áreas de la nanomedicina, como p.
Una corona de proteínas se forma cuando las nanopartículas entran en la sangre humana y entran en contacto con varias biomoléculas como proteínas, lípidos, ácidos nucleicos, metabolitos y azúcares. El recubrimiento de la superficie de las nanopartículas que forman estas biomoléculas se denomina proteína biomolecular corona.
Su importancia para aplicaciones biomédicas, p. B. la administración de fármacos en nanomedicina radica en su función de dar a la nanopartícula una identidad biológica única que podría ser muy diferente de la superficie original de la nanopartícula.
La naturaleza compleja de la composición de la proteína corona tiene implicaciones significativas para la biodistribución, la eficacia de la orientación y también la toxicidad, ya que la proteína corona confiere una nueva identidad biológica a las nanopartículas. En otras palabras, la proteína corona es el “lado visible” de las nanopartículas y, por lo tanto, tiene un impacto significativo en la en vivo Vecindad.
El hecho de que las propiedades de una nanopartícula terapéutica puedan cambiar, hasta un punto desconocido, simplemente introduciéndola en el cuerpo genera importantes desafíos científicos y tecnológicos en el diseño y desarrollo de nanomateriales para aplicaciones diagnósticas y terapéuticas.
Esto significa que comprender la interacción de las biomoléculas en la corona biomolecular con la superficie de las nanopartículas es esencial para la seguridad y eficacia diagnóstica y terapéutica de los nanomedicamentos.
«La caracterización robusta de la identidad y la abundancia de la proteína corona depende completamente de la cromatografía líquida junto con la espectroscopia de masas (LC-MS/MS)», le dice a Nanowerk Morteza Mahmoudi, profesora asistente en el Programa de Salud de Precisión de la Universidad Estatal de Michigan. «Desafortunadamente, la variabilidad de esta técnica con el fin de caracterizar las coronas de proteínas aún no se conoce bien».
Para mejorar esta situación, Mahmoudi y su equipo investigaron la variabilidad de los flujos de trabajo de LC-MS en los resultados de la corona de proteínas enviando 17 alícuotas idénticas de coronas de proteínas a diferentes instalaciones de proteómica central en los EE. UU. y analizando los conjuntos de datos recuperados.
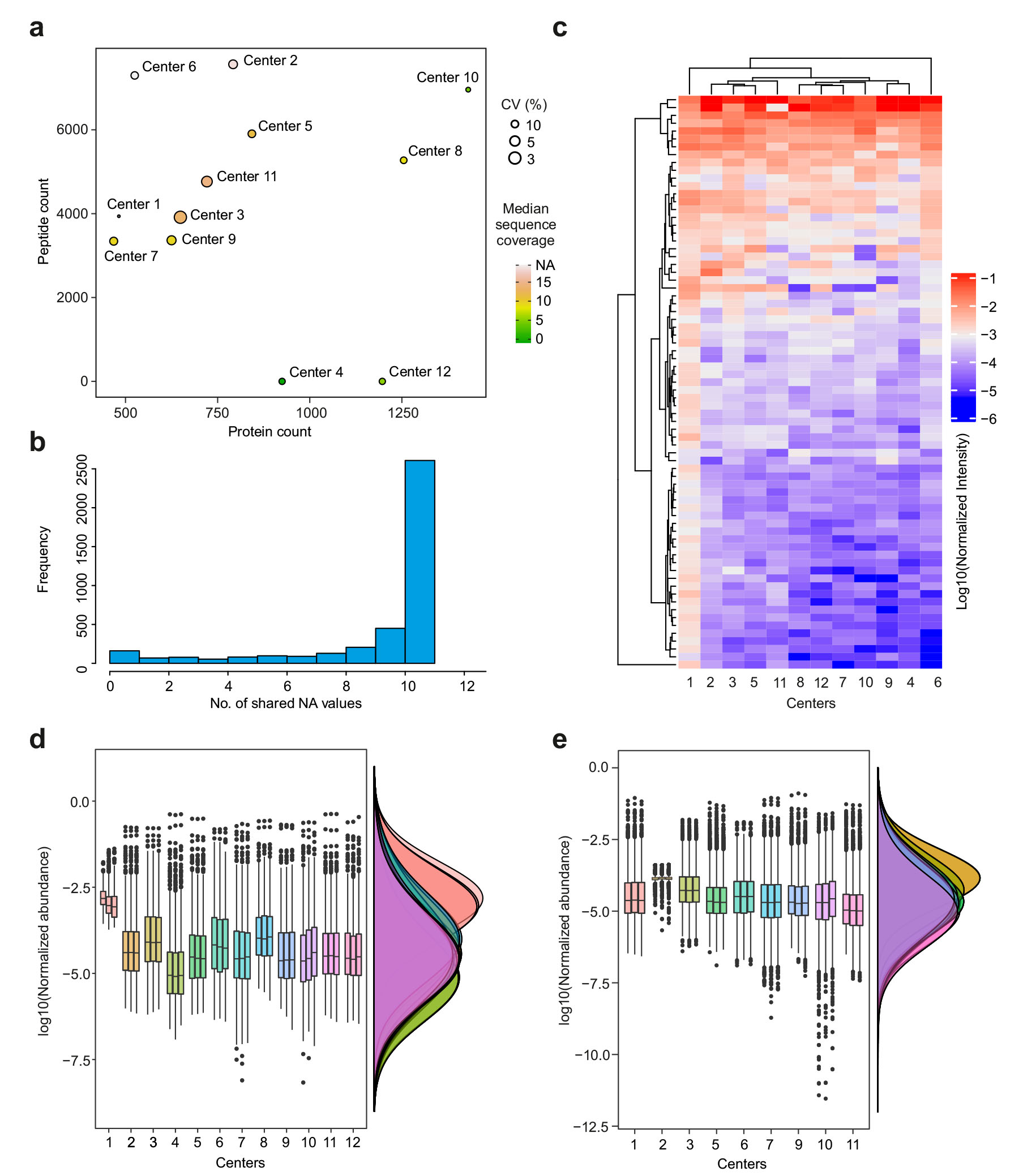
Descubrieron que aunque los datos compartidos se correlacionan bien entre los núcleos, existe una heterogeneidad significativa en los datos recuperados de diferentes núcleos. Sorprendentemente, de las 4022 proteínas únicas identificadas, solo 73 (1,8 %) se compartieron entre diferentes instalaciones centrales.
Los resultados informados en comunicación de la naturaleza («Medidas de heterogeneidad en el análisis proteómico de corona de proteína de nanopartículas en instalaciones centrales»), aumentan el impacto crítico de los detalles de LC-MS, p. B. Protocolo de preparación de muestras, instrumentación y procesamiento de datos sin procesar: afectan los resultados de corona de proteínas que pueden introducir sesgos en la interpretación de las aplicaciones de corona de proteínas, incluido el descubrimiento de biomarcadores y el destino biológico de las tecnologías de nanomedicina.
Estos resultados demuestran que los conjuntos de datos de proteína-corona no se pueden comparar fácilmente entre estudios independientes y comprometen la interpretación de la investigación de proteína-corona de manera más amplia, con implicaciones para el descubrimiento de biomarcadores y la seguridad y eficacia de las biotecnologías a nanoescala.
El equipo de Mahmoudi informó anteriormente sobre varios factores pasados por alto en las nanobiointerfaces y la composición de la corona de proteínas, como la cantidad y el tipo de proteínas, que es uno de los puntos críticos para predecir la seguridad, la biodistribución y la eficacia diagnóstica/terapéutica de los dispositivos de nanomedicina. (Lea más en nuestro anterior emisor nanowerk: «Explorando el papel crucial de las coronas biomoleculares en las interacciones nanopartícula-célula»; «Las coronas de proteínas personalizadas conducen a diferentes efectos terapéuticos o tóxicos de nanopartículas idénticas» y «Caracterización de la corona biomolecular a nivel de nanopartículas individuales»).
«Actualmente, la caracterización de la corona de proteínas en términos de tipos y abundancia de proteínas depende completamente de una sola técnica (es decir, LC-MS), y los resultados de la corona de proteínas y las interpretaciones correspondientes son diferentes cuando se utilizan diferentes LC-MS. instrumentación», dice Mahmoudi, «Lo que encontramos en nuestro estudio es que existe una variación notable en la composición de la corona de proteínas de nanopartículas similares, incluso en condiciones experimentales similares en términos de número de proteínas, tipo de proteínas, abundancia de proteínas, etc. »
«Nuestros resultados indican que existe una necesidad urgente de desarrollar un protocolo estándar y flujos de trabajo para el análisis corona de proteínas en términos de preparación y análisis de muestras LC-MS/MS para minimizar la heterogeneidad de los resultados finales», agrega.
Una de las posibles próximas fases de esta investigación sería el desarrollo de un protocolo estándar de LC-MS y su envío a diferentes instalaciones centrales/centros de proteómica para caracterizar la composición de la corona de proteínas con el fin de minimizar la heterogeneidad de los resultados de la corona de proteínas en el núcleo. instalaciones.
Mahmoudi reconoce que desarrollar un protocolo estándar único para el análisis LC-MS estándar y convencer a los laboratorios de proteómica central para que sigan los mismos procedimientos para el análisis de corona de proteínas sería un desafío importante: las diferentes instalaciones centrales y centros de proteómica no tienen acceso a los mismos instrumentos (p. espectrómetros de masas y sistemas de cromatografía), el mismo software (p. ej., software comercial de búsqueda de bases de datos), ni podrían seguir los protocolos precisos que se indican a continuación (p. ej., uso de diferentes enzimas para la digestión, agentes reductores, protocolos de purificación, etc.). Además, también sería imposible medir el grado de conformidad con el protocolo, p. B. Tiempos de incubación, calidad de los materiales utilizados, etc.
“Durante la última década, hemos visto un éxito limitado en la administración clínica de nanopartículas terapéuticas, y una de las razones principales de esta limitación es la heterogeneidad de los resultados de la corona de proteínas en el campo debido a la composición compleja de la corona de proteínas y la falta de un protocolo/enfoque estándar para caracterizar e interpretar los perfiles corona de proteínas», concluye Mahmoudi. «La depuración de estos factores pasados por alto conducirá a una comprensión más profunda de la identidad biológica de las nanopartículas. en vivo ambientes».
Miguel
Berger
–
Michael es autor de tres libros de la Royal Society of Chemistry: Nano-Society: Pushing the Boundaries of Technology, Nanotechnology: The Future is Tiny y Nanoengineering: The Skills and Tools Making Technology Invisible Copyright ©
Nanowerk
¡Conviértase en un escritor invitado de Spotlight! Únase a nuestro grupo grande y creciente de escritores invitados. ¿Acaba de publicar un artículo científico o tiene otros avances interesantes que le gustaría compartir con la comunidad de nanotecnología? Cómo publicar en nanowerk.com.
[ad_2]

