[ad_1]
(noticias nanowerk) Una reacción química clave, en la que el movimiento de protones entre la superficie de un electrodo y un electrolito impulsa una corriente eléctrica, es un paso crucial en muchas tecnologías energéticas, incluidas las pilas de combustible y los electrolizadores para producir gas hidrógeno.
Por primera vez, químicos del MIT han detallado cómo se producen estas transferencias de electrones acoplados a protones en la superficie de un electrodo. Sus resultados podrían ayudar a los investigadores a desarrollar pilas de combustible, baterías u otras tecnologías energéticas más eficientes.
«Nuestro progreso en este trabajo ha sido estudiar y comprender la forma en que estos electrones y protones se acoplan a una superficie, lo cual es relevante para reacciones catalíticas importantes en el contexto de dispositivos de conversión de energía o reacciones catalíticas», dice Yogesh Surendranath, profesor de química. e ingeniería química en el MIT y autor principal del estudio.
Entre otras cosas, los investigadores pudieron controlar de cerca cómo los cambios en el pH de la solución electrolítica que rodea un electrodo afectan la velocidad del movimiento de los protones y el flujo de electrones dentro del electrodo.
Noah Lewis, graduado del MIT, es el autor principal del artículo, que aparece hoy en quimica natural (“Un marco mecanicista a nivel molecular para la cinética de la transferencia de electrones acoplados a protones en la interfaz”). Ryan Bisbey, ex postdoctorado del MIT; Karl Westendorff, graduado del MIT; y Alexander Soudackov, científico investigador de la Universidad de Yale, también son autores del artículo.
Protones pasando
La transferencia de electrones acoplados a protones ocurre cuando una molécula, a menudo agua o un ácido, transfiere un protón a otra molécula o a la superficie de un electrodo, estimulando al aceptor de protones para que también acepte un electrón. Este tipo de reacción se ha utilizado para muchas aplicaciones energéticas.
“Estas reacciones de transferencia de electrones acoplados a protones son omnipresentes. A menudo son pasos clave en los mecanismos catalíticos y son particularmente importantes para los procesos de conversión de energía, como la producción de hidrógeno o la catálisis de pilas de combustible”, afirma Surendranath.
En un electrolizador productor de hidrógeno, este enfoque se utiliza para eliminar protones del agua y agregar electrones a los protones para formar gas hidrógeno. En una pila de combustible, la electricidad se produce cuando se eliminan protones y electrones del gas hidrógeno y se mezclan con oxígeno para formar agua.
La transferencia de electrones acoplados a protones es común en muchos otros tipos de reacciones químicas, como la reducción de dióxido de carbono (la conversión de dióxido de carbono en combustibles químicos mediante la adición de electrones y protones). Los científicos han aprendido mucho sobre cómo ocurren estas reacciones cuando los aceptores de protones son moléculas, ya que pueden controlar con precisión la estructura de cada molécula y observar cómo pasan electrones y protones entre ellas. Sin embargo, cuando la transferencia de electrones acoplados a protones ocurre en la superficie de un electrodo, el proceso es mucho más difícil de estudiar porque las superficies de los electrodos suelen ser muy heterogéneas y tienen muchos sitios diferentes a los que potencialmente podría unirse un protón.
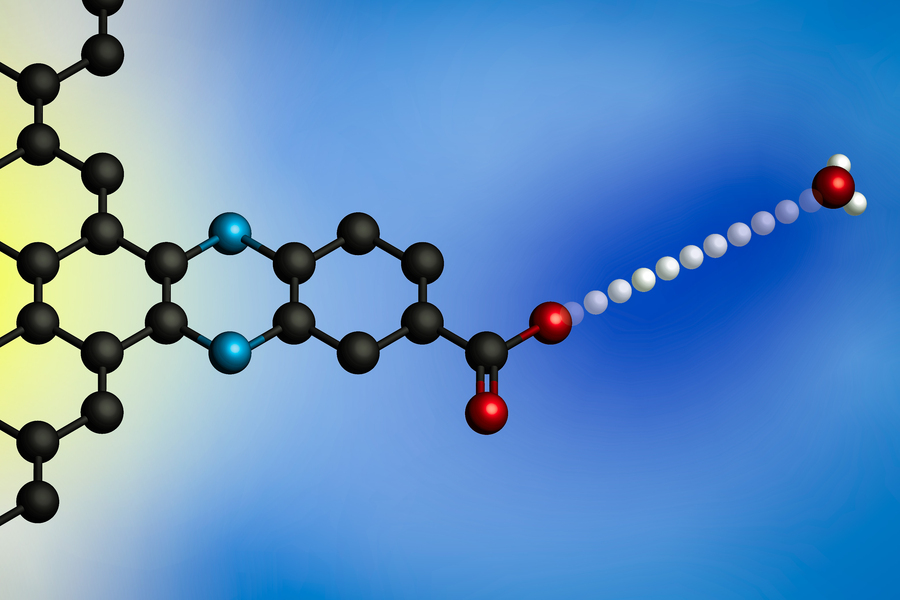
Para superar este obstáculo, el equipo del MIT desarrolló un método para diseñar superficies de electrodos que les permite un control mucho más preciso sobre la composición de la superficie del electrodo. Sus electrodos consisten en capas de grafeno con compuestos orgánicos que contienen anillos adheridos a la superficie. Al final de cada una de estas moléculas orgánicas hay un ion de oxígeno cargado negativamente que puede aceptar protones de la solución circundante, lo que hace que un electrón fluya desde el circuito hacia la superficie del grafito.
«Podemos crear un electrodo que no esté formado por una gran variedad de sitios, sino que sea una matriz uniforme de un solo tipo de sitios muy bien definidos, cada uno de los cuales puede unirse a un protón con la misma afinidad», dice Surendranath. «Debido a que tenemos estas ubicaciones muy bien definidas, pudimos desentrañar realmente la cinética de estos procesos».
Este sistema permitió a los investigadores medir el flujo de corriente a los electrodos y así calcular la tasa de transferencia de protones al ion oxígeno en la superficie en equilibrio: el estado en el que la tasa de entrega de protones a la superficie es alta y la transferencia de protones desde la superficie en las soluciones es la misma. Descubrieron que el pH de la solución circundante tenía un impacto significativo en esta tasa: las tasas más altas se produjeron en los extremos de la escala de pH: pH 0, el más ácido, y pH 14, el más básico.
Para explicar estos resultados, los investigadores desarrollaron un modelo basado en dos posibles reacciones que pueden ocurrir en el electrodo. En el primer caso, los iones hidronio (H3oh+), que se encuentran en altas concentraciones en soluciones fuertemente ácidas, liberan protones a los iones de oxígeno en la superficie y producen así agua. En el segundo caso, el agua dona protones a los iones de oxígeno de la superficie, creando iones de hidróxido (OH).–), que están presentes en altas concentraciones en soluciones fuertemente básicas.
Sin embargo, la velocidad a pH 0 es aproximadamente cuatro veces más rápida que a pH 14, en parte porque el hidronio libera protones más rápido que el agua.
Una reacción para repensar
Para su sorpresa, los investigadores también descubrieron que las dos reacciones tienen velocidades iguales, no a un pH neutro de 7, donde las concentraciones de hidronio e hidróxido son iguales, sino a un pH de 10, donde la concentración de iones de hidróxido es un millón de veces mayor como la del hidronio. . El modelo sugiere que esto se debe a que la reacción directa con la donación de protones mediante hidronio o agua contribuye más a la velocidad general que la reacción inversa con la eliminación de protones mediante agua o hidróxido.
Los modelos existentes sobre cómo ocurren estas reacciones en las superficies de los electrodos suponen que las reacciones directa e inversa contribuyen por igual a la velocidad general. Por lo tanto, los nuevos hallazgos sugieren que es posible que sea necesario reconsiderar estos modelos, dicen los investigadores.
«Esta es la suposición estándar de que las reacciones hacia adelante y hacia atrás contribuyen por igual a la velocidad de reacción», dice Surendranath. «Nuestro hallazgo es realmente revelador porque significa que es posible que debamos repensar las suposiciones con las que la gente analiza todo, desde la catálisis de las pilas de combustible hasta la evolución del hidrógeno».
Con su configuración experimental, los investigadores ahora están investigando cómo agregar diferentes tipos de iones a la solución electrolítica alrededor del electrodo puede acelerar o disminuir la velocidad del flujo de electrones acoplados a protones.
«Con nuestro sistema, sabemos que nuestras ubicaciones son constantes y no se afectan entre sí, por lo que podemos descubrir qué efecto tiene el cambio en la solución sobre la reacción en la superficie», dice Lewis.
[ad_2]

