[ad_1]
Utilizando sofisticados métodos de medición basados en microscopía óptica de campo cercano, un equipo de investigación interdisciplinario del Instituto de Ciencia Molecular dirigido por Jun Nishida (profesor asistente) y Takashi Kumagai (profesor asociado) logró observar espectros vibratorios de proteínas individuales, que constan de varios proteínas formadas por unos 500 residuos de aminoácidos.
El logro representa un importante paso adelante en el desarrollo de avances técnicos como la obtención de imágenes infrarrojas de alta sensibilidad y alta resolución y la espectroscopia vibratoria de una sola molécula.
Debido a que la espectroscopia infrarroja puede cuantificar espectros vibratorios, a menudo denominados “huellas dactilares moleculares”, se utiliza ampliamente para el estudio estructural y químico de una variedad de materiales. Debido al rápido crecimiento reciente de la nanotecnología, existe una mayor demanda de imágenes infrarrojas de ultra alta sensibilidad y alta resolución.
Sin embargo, detectar muestras diminutas o lograr una resolución espacial a nanoescala supera las capacidades de la espectroscopia infrarroja convencional. Por ejemplo, es difícil cuantificar una sola proteína porque la microespectroscopia infrarroja extremadamente sensible requiere más de un millón de proteínas para producir un espectro infrarrojo.
La nueva técnica utiliza luz confinada a la nanoescala, lo que permite un análisis detallado de muestras muy pequeñas, algo difícil de lograr con la espectroscopia infrarroja tradicional.
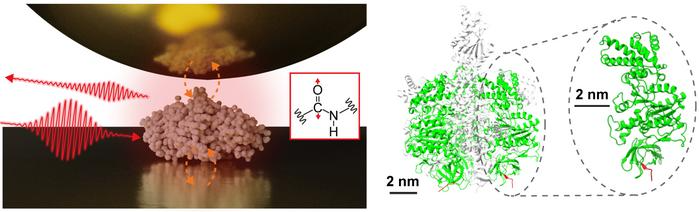
Los investigadores utilizaron un sustrato de oro para aislar una sola proteína (una subunidad de un complejo proteico llamado F1-ATPasa) y luego realizaron estudios de espectroscopia infrarroja de campo cercano en un entorno natural. Hicieron avances significativos al capturar eficazmente el espectro vibratorio infrarrojo de una sola proteína, lo que podría ayudar a caracterizar las organizaciones estructurales locales de proteínas específicas.
Con conocimientos mejorados sobre los procesos y las interacciones de las proteínas de membrana y los complejos de proteínas, esta información es particularmente importante para comprender sus intrincadas funciones. Además, se creó un novedoso marco teórico que explica las interacciones a nanoescala entre la proteína y el campo cercano infrarrojo.
Utilizando la teoría, el grupo pudo reproducir estadísticamente los espectros de vibración experimentales observados. Estos hallazgos abrirán la puerta a diversas aplicaciones de la espectroscopia infrarroja a nanoescala, incluido el estudio químico de biomoléculas y otros nanomateriales.
Referencia de la revista:
Nishida, J., et. Alabama. (2023) Interacciones de campo cercano del radio de la punta secundaria en espectroscopia vibratoria nano-FTIR en proteínas individuales. nano letras. doi:10.1021/acs.nanolett.3c03479.
Fuente: https://www.nins.jp/en/
[ad_2]

