[ad_1]
(Foco Nanowerk) La detección temprana del cáncer es fundamental para un tratamiento eficaz y mejorar los resultados de los pacientes. Un desafío clave es encontrar formas de detectar pequeñas cantidades de células tumorales circulantes (CTC) en muestras de sangre. Las CTC se han desprendido del sitio del tumor original y han entrado en el torrente sanguíneo. Sirven como señal de advertencia temprana de que el cáncer puede estar propagándose a otras áreas del cuerpo o haciendo metástasis.
La capacidad de detectar con precisión CTC a partir de una extracción de sangre estándar podría permitir a los oncólogos diagnosticar cánceres antes, seleccionar terapias dirigidas y monitorear la efectividad del tratamiento.
Sin embargo, las CTC se producen con frecuencias extremadamente bajas entre miles de millones de células sanguíneas normales. Este problema de la aguja en un pajar dificulta identificar y aislar claramente las CTC para su posterior análisis. Las plataformas actuales de detección de CTC tienen dificultades para distinguir las CTC de la gran cantidad de glóbulos blancos presentes. Como resultado, las muestras aisladas todavía contienen altos niveles de “contaminantes” de glóbulos blancos, lo que dificulta el perfilado genómico o proteómico de las escasas CTC.
Para mejorar la pureza del aislamiento de CTC, científicos de la Universidad de Nankai en China han desarrollado nanopartículas magnéticas (MN) recubiertas con membranas celulares que explotan las capacidades especiales de dos tipos de células diferentes. Como informa la revista Materiales funcionales avanzados (“Nanopartículas magnéticas recubiertas de membrana celular diseñadas genéticamente para el aislamiento de alto rendimiento de células tumorales circuladas”), las nanopartículas biomiméticas del equipo pueden atacar específicamente las CTC y evitar la unión no específica a los glóbulos blancos.
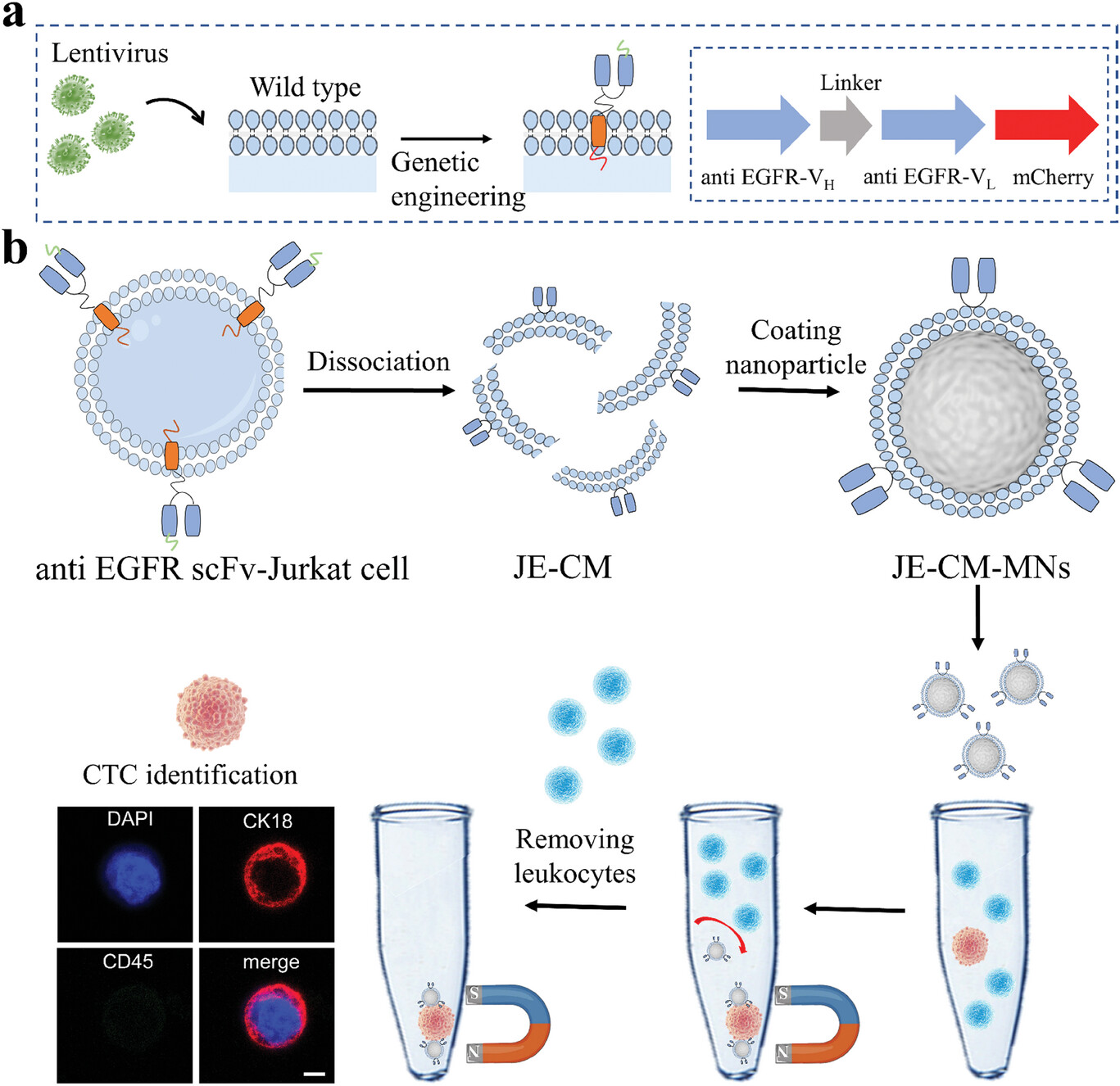
Los investigadores recubren núcleos de nanopartículas magnéticas con membranas celulares extraídas de células inmunes Jurkat. Este camuflaje de la membrana de los leucocitos permite que las partículas evadan la detección de los glóbulos blancos, de forma similar a cómo los virus utilizan una cubierta de membrana para penetrar de forma invisible en las células huésped. Las pruebas demostraron que las nanopartículas camufladas tenían muchas menos interacciones con los glóbulos blancos en comparación con las nanopartículas desnudas en muestras de sangre.
«La membrana celular juega un papel esencial en muchos procesos fisiológicos y patológicos», afirmó el Dr. Lailiang Ou, autor principal del artículo. «Estudios recientes han demostrado que el recubrimiento de la membrana leucocitaria puede reducir la interacción entre las partículas y los leucocitos, lo que puede considerarse un recubrimiento de camuflaje ideal contra las células homólogas».
Al mismo tiempo, el equipo muestra fragmentos de anticuerpos variables de cadena sencilla (scFv) en las superficies de las nanopartículas que se dirigen al receptor del factor de crecimiento epidérmico, una proteína que a menudo se sobreexpresa en las células cancerosas. Esta tecnología de membrana de anticuerpos quiméricos se logró modificando genéticamente las células Jurkat para expresar de manera estable el scFv cazador de tumores en su membrana externa. Al extruir las membranas celulares diseñadas sobre nanopartículas magnéticas, esta capacidad de captura selectiva de CTC se transfirió a las nanopartículas.
Modificando la membrana celular y luego recubriendo las nanopartículas con ella, el equipo pudo dotar a las nanopartículas tanto de la capacidad de evadir los glóbulos blancos como de capacidades específicas para apuntar a CTC.
Para probar el rendimiento de las nanopartículas diseñadas, los investigadores agregaron (o agregaron) cantidades conocidas de células cancerosas a muestras de sangre de donantes sanos. Esto creó muestras de sangre artificiales que contenían números controlados de células cancerosas para imitar extracciones de sangre clínicas reales.
Luego, las nanopartículas manipuladas se agregaron a estas muestras de sangre enriquecidas. En comparación con las nanopartículas comerciales dirigidas a CTC probadas en las mismas muestras con aditivos añadidos, las nuevas nanopartículas se dirigieron a un número significativamente mayor de células cancerosas: 80 % frente al 52 % de las nanopartículas comerciales. Curiosamente, el recubrimiento de la membrana celular redujo simultáneamente el fondo de glóbulos blancos a solo el 7% de todas las células aisladas, lo que representa una mejora de casi diez veces en la pureza.
«Nuestra plataforma demostró una excelente especificidad y una detección sensible en muestras de sangre clínicas, lo que permite un diagnóstico conveniente del cáncer en pacientes con una tasa de detección del 100 %», explicó el Dr. Xinglu Huang, coautor del estudio.
La capacidad de detectar CTC de forma no invasiva con alto rendimiento y pureza podría resultar de gran ayuda para la detección temprana del cáncer y el seguimiento del tratamiento. Se requiere una validación adicional con muestras de pacientes más grandes antes de la implementación clínica. También existe la posibilidad de ampliar el enfoque apuntando a diferentes proteínas de membrana que se sobreexpresan en diferentes tipos de cáncer. Esta innovadora plataforma de nanopartículas biomiméticas representa una nueva táctica prometedora en la lucha contra el cáncer metastásico.

De
Miguel
Berger
– Michael es autor de tres libros de la Royal Society of Chemistry: Nano-Society: Pushing the Boundaries of Technology, Nanotechnology: The Future is Tiny y Nanoengineering: The Skills and Tools Making Technology Invisible Copyright ©
Nanowerk LLC
¡Conviértete en autor invitado de Spotlight! Únase a nuestro gran y creciente grupo de autores invitados. ¿Acaba de publicar un artículo científico o le gustaría compartir otros desarrollos interesantes con la comunidad de nanotecnología? Cómo publicar en nanowerk.com.
[ad_2]

