[ad_1]
(noticias nanowerk) Investigadores de la Universidad de Toronto han desarrollado una nueva teoría para explicar cómo las nanopartículas entran y salen de los tumores para los que están diseñadas. Al hacerlo, es posible que los investigadores hayan redefinido la comprensión de la nanomedicina contra el cáncer que ha guiado la investigación durante casi cuatro décadas.
El efecto de permeabilidad y retención mejoradas (EPR), un concepto prácticamente indiscutido desde mediados de la década de 1980, supone que las nanopartículas del torrente sanguíneo ingresan al tumor a través de espacios entre las células endoteliales que recubren sus vasos sanguíneos, y luego, debido a ello, se incluyen vasos linfáticos disfuncionales. en el tumor.
«El aspecto de retención de la teoría EPR depende de que la cavidad del vaso linfático sea demasiado pequeña para que escapen las nanopartículas, lo que permite que las nanopartículas que contienen medicamentos contra el cáncer permanezcan en los tumores», dijo Matthew Nguyen, estudiante de posgrado en el Instituto de Ingeniería Biomédica. en la Facultad de Ciencias Aplicadas e Ingeniería y el Centro Donnelly de Investigación Celular y Biomolecular,
«Pero hemos descubierto que alrededor del 45 por ciento de las nanopartículas que se acumulan en los tumores también salen de ellos».
Nguyen, miembro del laboratorio del profesor Warren Chan, es el autor principal de un nuevo estudio que desafía la teoría de larga data, publicado recientemente en la revista Materiales naturales (“El escape de nanopartículas de tumores sólidos”). Los hallazgos de los investigadores ayudan a explicar por qué los tratamientos basados en el efecto EPR fracasan en los ensayos clínicos. Se basan en investigaciones anteriores del laboratorio Chan que demostraron que menos del uno por ciento de las nanopartículas llegan realmente a los tumores.
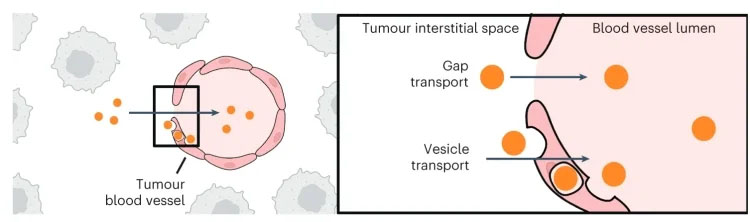
Los investigadores descubrieron que, a diferencia del efecto EPR, las nanopartículas pueden salir de los tumores a través de los vasos linfáticos. El método de salida de una nanopartícula depende de su tamaño: las más grandes (de 50 a 100 nanómetros de ancho) tienen más probabilidades de salir a través de los vasos linfáticos de los tumores, mientras que las más pequeñas (de hasta 15 nanómetros de ancho) tienen más probabilidades de salir a través de los vasos linfáticos. vasos que rodean los tumores.
En casos raros, las nanopartículas se filtrarán a través de los vasos sanguíneos.
El escape de las nanopartículas de los tumores se produce a través de espacios en las paredes de los vasos linfáticos y vesículas de transporte que las transportan a través de estas paredes. Los investigadores demostraron que las nanopartículas vuelven a ingresar al torrente sanguíneo después del drenaje linfático y plantearon la hipótesis de que estas nanopartículas eventualmente regresan al tumor para tratarlo nuevamente.
Refutar el efecto EPR no fue una tarea fácil. El laboratorio Chan pasó seis años intentando comprender por qué las nanopartículas no se acumulan eficazmente en los tumores. Antes de este estudio, el laboratorio se centró inicialmente en cómo las nanopartículas llegan a los tumores. A través de estos y otros estudios, el laboratorio desarrolló una teoría competitiva sobre el efecto EPR, llamada principio de retención y transporte activo (ATR).
Nguyen señaló que el campo de la nanomedicina ha evolucionado desde que se publicó el estudio de entrada de nanopartículas en 2020. «Recibimos más rechazo de otros investigadores en este estudio que en este», dijo. «La gente está empezando a aceptar que el efecto EPR es defectuoso».
Debido a que casi la mitad de las nanopartículas acumuladas salen de los tumores, principalmente a través de los vasos linfáticos, investigaciones futuras podrían abordar este problema mediante tratamientos con nanopartículas que impidan el drenaje linfático.
«Estamos entusiasmados de comprender mejor el proceso de administración de tumores con nanopartículas», dijo Chan. «Los resultados de estos estudios fundamentales sobre la entrada y salida de nanopartículas serán importantes para el desarrollo de nanopartículas para tratar el cáncer».
Si los resultados del estudio se aplican a todo el campo de la nanomedicina contra el cáncer, prometen una nueva dirección para mejorar nuestra comprensión de cómo se pueden utilizar las nanopartículas para tratar tumores.
«Tratar de trasladar la nanomedicina contra el cáncer a la clínica es como trabajar con una caja negra: algunos medicamentos funcionan, otros no, y es difícil saber por qué», afirmó Gang Zheng, subdirector de investigación del Centro Oncológico Princess Margaret y profesor de biofísica médica en la Facultad de Medicina Temerty de la U of T que no participó en el estudio.
«El compromiso de Chan de comprender mejor los mecanismos de absorción y salida de nanopartículas arroja luz sobre estos procesos y ayudará a que nuestros esfuerzos de traducción sean más eficientes y exitosos».
[ad_2]

