[ad_1]
(Foco Nanowerk) Desde el descubrimiento de la doble hélice del ADN en 1953, los investigadores han soñado con utilizar ácidos nucleicos para aplicaciones biomédicas revolucionarias que beneficien la salud humana. Los primeros visionarios imaginaron el desarrollo de ADN y ARN como biosensores para detectar toxinas, como vectores para terapias génicas y con nanopartículas cargadas de fármacos para una administración de fármacos dirigida con precisión.
Sin embargo, surgieron obstáculos formidables. Cuando se inyectaron en modelos animales, los ácidos nucleicos sintéticos desencadenaron un ataque inmunológico agresivo que colapsó antes de que se lograra un efecto terapéutico. Las dosis altas desencadenaron cascadas inflamatorias o toxicidad que provocaron daño a los órganos.
Como resultado, los expertos se volvieron escépticos de que los ácidos nucleicos tuvieran alguna promesa como tecnología. Sin embargo, algunos científicos persistentes exploraron nuevas configuraciones estructurales y modificaciones químicas y poco a poco descubrieron cómo mejorar la biocompatibilidad.
En la década de 2000, los ácidos nucleicos ganaron una tracción limitada: la interferencia de ARN permitió el silenciamiento genético experimental y las nanopartículas esféricas de ácido nucleico demostraron una mejor administración de fármacos sin inflamación. Sin embargo, las nanofibras de ácido nucleico alargadas con una alta relación de aspecto y una mayor capacidad funcional seguían siendo difíciles de alcanzar. Cuando se introducen por vía intravenosa, estos filamentos activan inmediatamente las cascadas del complemento que marcan el material extraño, provocando así una rápida eliminación.
Ahora, en 2024, la búsqueda de décadas para equilibrar la eficacia, la seguridad y la programabilidad de las nanotecnologías de ácidos nucleicos (es decir, la nanotecnología de ADN y la nanotecnología de ARN) puede haber llegado a un punto de inflexión.
Un equipo de investigación dirigido por el Laboratorio Afonin de la UNC Charlotte descubrió recientemente un mecanismo elegante para regular las respuestas inmunitarias desencadenadas por nanofibras de ácido nucleico en forma de varilla cuando se introducen en células humanas.
Los resultados del equipo fueron publicados en Interfaces y materiales aplicados de ACS (“Immunostimulation of Fibrous Nucleic Acid Nanoparticles Can be Modulated Through Aptamer-Based Functional Moieties: Unveiling the Structure-Activity Relationship and Mechanistic Insights”) describe una técnica para camuflar las propiedades inmunoestimuladoras de los andamios de nanofibras de ácido nucleico mediante la decoración de aptámeros de ADN, ampliando así las posibilidades. para utilizar estructuras como adyuvantes de vacunas o vectores de inmunoterapia que requieren una activación inmune controlada.
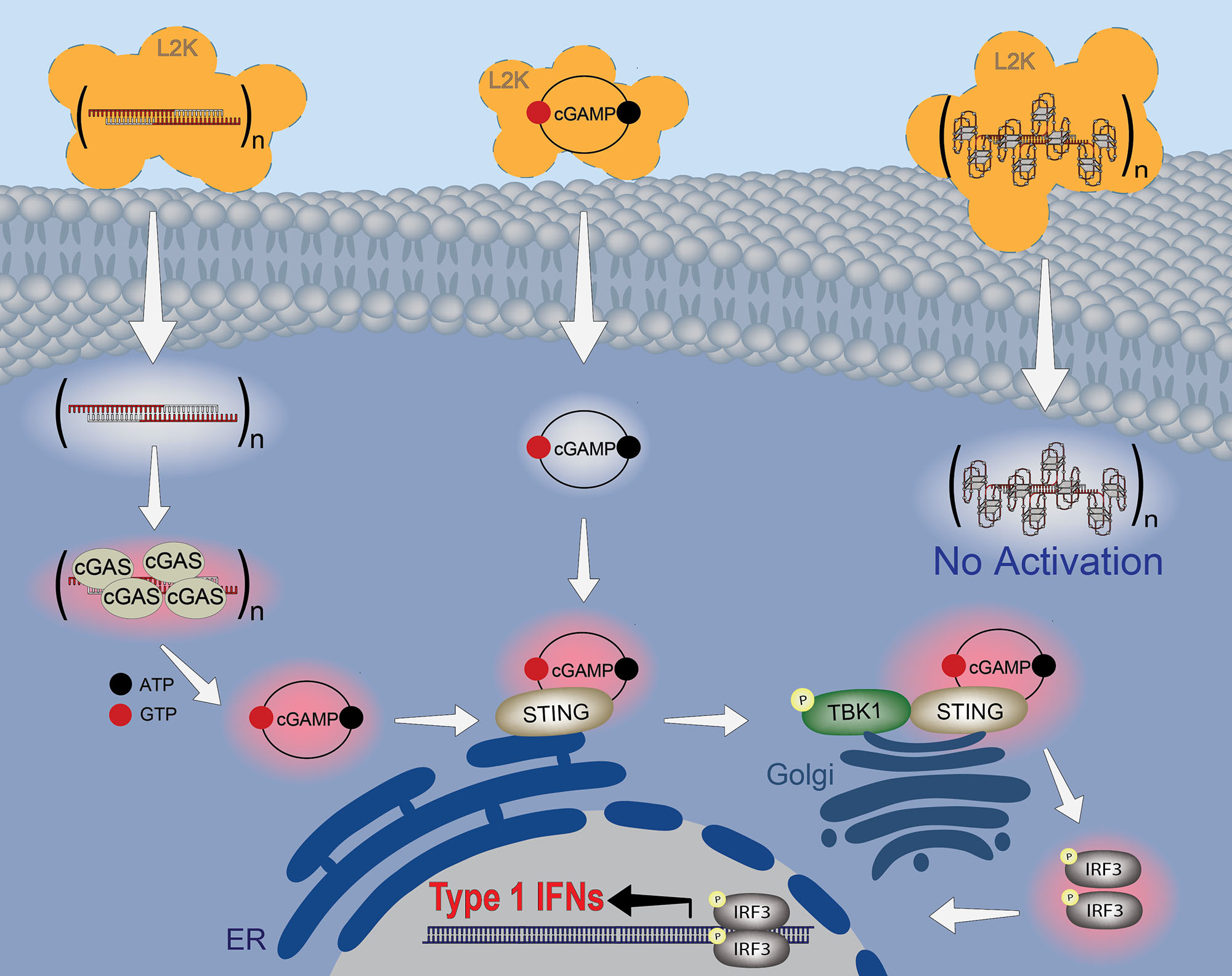
Este descubrimiento amplía fundamentalmente la capacidad del campo para regular las respuestas inmunes desencadenadas por ácidos nucleicos producidos sintéticamente. Al dilucidar un elegante mecanismo biomolecular que rodea a la proteína sensora inmune innata cGAS, los investigadores han definido una solución de ingeniería para disfrazar la inmunogenicidad de las nanofibras de ácido nucleico en forma de varilla que requieren administración intracelular para funcionar.
Desde su descubrimiento inicial en la década de 1980, el ARN y el ADN sintéticos se han transformado en nanoarquitecturas 3D personalizadas que exhiben propiedades deseables, como propiedades mejoradas. en vivo Capacidad circulatoria y biodistribución o mayor eficiencia de carga de carga molecular en comparación con estructuras lineales. Por ello, los expertos reconocieron un enorme potencial de aplicación si se pudiera lograr de forma fiable una regulación adecuada de los efectos secundarios inflamatorios indeseables y de la toxicidad de las nanopartículas.
Los esfuerzos iniciales en la década de 2000 tenían como objetivo superar las complicaciones asociadas con el estrés oxidativo inducido por nanopartículas y las cascadas inflamatorias posteriores, centrándose casi exclusivamente en nanoestructuras esféricas de ácidos nucleicos.
Sin embargo, la fisiología beneficiosa que ofrecen las arquitecturas en forma de varilla de alta relación de aspecto sigue siendo tentadora pero difícil de alcanzar. Sólo en los últimos años, sofisticadas nanofibras de ADN y ARN han permitido un rápido control de la coagulación sanguínea, la regeneración sináptica después de una lesión neuronal y logros sin precedentes. en vivo Tiempos de circulación.
Sin embargo, una vez internalizada en las células, la morfología alargada y los patrones superficiales repetitivos parecen confundir al sistema inmunológico innato y provocarlo, como si estuviera luchando contra una peligrosa invasión de patógenos, cuando tal respuesta resulta ser completamente innecesaria y francamente dañina.
«Presumimos que podríamos resolver este rompecabezas mediante una estrategia de pasivación de la estructura, esencialmente camuflando la estructura de ácido nucleico subyacente decorando toda la superficie con aptámeros de ADN personalizados para que el sistema inmunológico innato ya no reconozca el material como extraño», dice Afonin nanoworks.
Los aptámeros de ADN consisten en hebras simples cortas de oligonucleótidos sintéticos que pueden plegarse en conformaciones 3D específicas y unirse a proteínas diana con alta selectividad y afinidad. Los investigadores incorporaron uno o dos aptámeros de ADN diferentes por unidad repetida a lo largo de las nanofibras y validaron su hipótesis experimentalmente, primero en cultivos celulares de laboratorio y luego mediante simulaciones moleculares.
Descubrieron que la proteína sensora citosólica cGAS (GMP-AMP sintasa cíclica) parece ser la principal responsable de reconocer las nanofibras de ácido nucleico desprotegidas y, posteriormente, desencadenar señales inflamatorias.
Sin embargo, cuando se funcionalizan densamente con aptámeros de ADN, muchas menos proteínas cGAS parecen ser capaces de unirse al núcleo de ácido nucleico efectivamente oculto. En consecuencia, la producción de citoquinas y las respuestas al interferón disminuyeron significativamente. Curiosamente, las secuencias de aptámeros de ADN en sí mismas no desencadenaron ninguna respuesta inmune significativa: sólo los andamios de ácido nucleico descubiertos alertaron las defensas de la célula.
Las simulaciones proporcionaron una resolución atomística crucial y detallaron cómo la decoración con aptámeros de ADN perjudica y reduce la unión de la proteína sensora citosólica cGAS (GMP-AMP cíclico sintasa), que desencadena cascadas de señalización inflamatoria en ciertas células humanas cuando las estructuras de ácido nucleico descubiertas rompen la membrana celular. Debido a que el cGAS es suprimido por la conjugación de aptámeros de superficie, los haces en forma de barril de hélices de ADN interconectadas permanecen estructuralmente persistentes pero evaden el reconocimiento inmunológico. Los resultados se mantuvieron consistentes en tres células diferentes de donantes de sangre humana.
Al dilucidar esta estrategia de evasión, los investigadores disiparon las preocupaciones de que el tráfico intracelular mejoraría inherentemente la inmunidad antiviral utilizando nanofibras de ácido nucleico funcionales.
En cambio, los virólogos ahora esperan desarrollar adyuvantes o vectores que utilicen estimulación inmune controlada adaptada a los aptámeros. Los inmunoterapeutas del cáncer imaginan de manera similar que los nanorods de ácido nucleico que mejoran las citoquinas podrían desencadenar respuestas inmunes antitumorales. Ambos campos planean investigar si los nanofilamentos de ácido nucleico administrados internamente a través de complejos aptámero-liposoma podrían escapar de la degradación lisosomal inmediata y así mejorar la presentación de antígenos.
Además, los neurocientíficos esperan utilizar estos descubrimientos fundamentales para diseñar vías nerviosas excepcionalmente alargadas que apoyen la regeneración acelerada después de una lesión traumática.
Este avance tiene enormes implicaciones para toda la biomedicina y marca el comienzo de una nueva generación de nanotecnologías de ácidos nucleicos terapéuticas más inteligentes que están perfectamente vinculadas a la biología humana.

De
Miguel
Berger
– Michael es autor de tres libros de la Royal Society of Chemistry: Nano-Society: Pushing the Boundaries of Technology, Nanotechnology: The Future is Tiny y Nanoengineering: The Skills and Tools Making Technology Invisible Copyright ©
Nanowerk LLC
¡Conviértete en autor invitado de Spotlight! Únase a nuestro gran y creciente grupo de autores invitados. ¿Acaba de publicar un artículo científico o le gustaría compartir otros desarrollos interesantes con la comunidad de nanotecnología? Cómo publicar en nanowerk.com.
[ad_2]