[ad_1]
(noticias nanowerk) La observación de estructuras biomoleculares mediante microscopía de fuerza atómica (AFM) y la visualización directa de la dinámica conformacional funcional en experimentos AFM de alta velocidad (HS-AFM) han avanzado significativamente en la comprensión de los procesos biológicos a nanoescala. En los experimentos, se coloca una muestra biológica sobre una superficie de soporte (sustrato AFM) y se escanea con la punta de una sonda para registrar la forma molecular y sus cambios dinámicos.
La observación de la dinámica de las proteínas bajo HS-AFM es un delicado equilibrio entre inmovilizar la estructura en la superficie de soporte y, al mismo tiempo, prevenir la interferencia excesiva de la inmovilización.
El proceso de colocar una muestra biomolecular en la superficie de soporte y controlar su fijación adecuada es un desafío al comienzo de cada observación AFM. La composición química del tampón puede cambiar las interacciones entre la muestra y el sustrato. Estas modificaciones de la superficie son a menudo cruciales para las observaciones exitosas de AFM de las estructuras de las proteínas y sus movimientos funcionales. Sin embargo, la orientación molecular de la muestra se desconoce a priori y es difícil de inferir a partir de análisis posteriores debido a la resolución espacial limitada de las imágenes.
Romain Amyot, Noriyuki Kodera y Holger Flechsig de la Universidad de Kanazawa han desarrollado un modelo físico para predecir la ubicación de estructuras biomoleculares en sustratos de AFM basándose en interacciones electrostáticas. El método tiene en cuenta los sustratos comúnmente utilizados en experimentos de AFM (mica, mica APTES, bicapas lipídicas) y considera las condiciones del tampón. En simulaciones por computadora, se examina una gran cantidad de posibles disposiciones moleculares en el sustrato AFM y se determina la ubicación más favorable evaluando las energías de interacción correspondientes. Además, el análisis permite predecir la estabilidad de la imagen durante el escaneo de la punta.
El equipo publicó sus resultados en Fronteras de las biociencias moleculares (“Predicción de la colocación de estructuras biomoleculares sobre sustratos AFM basándose en interacciones electrostáticas”).
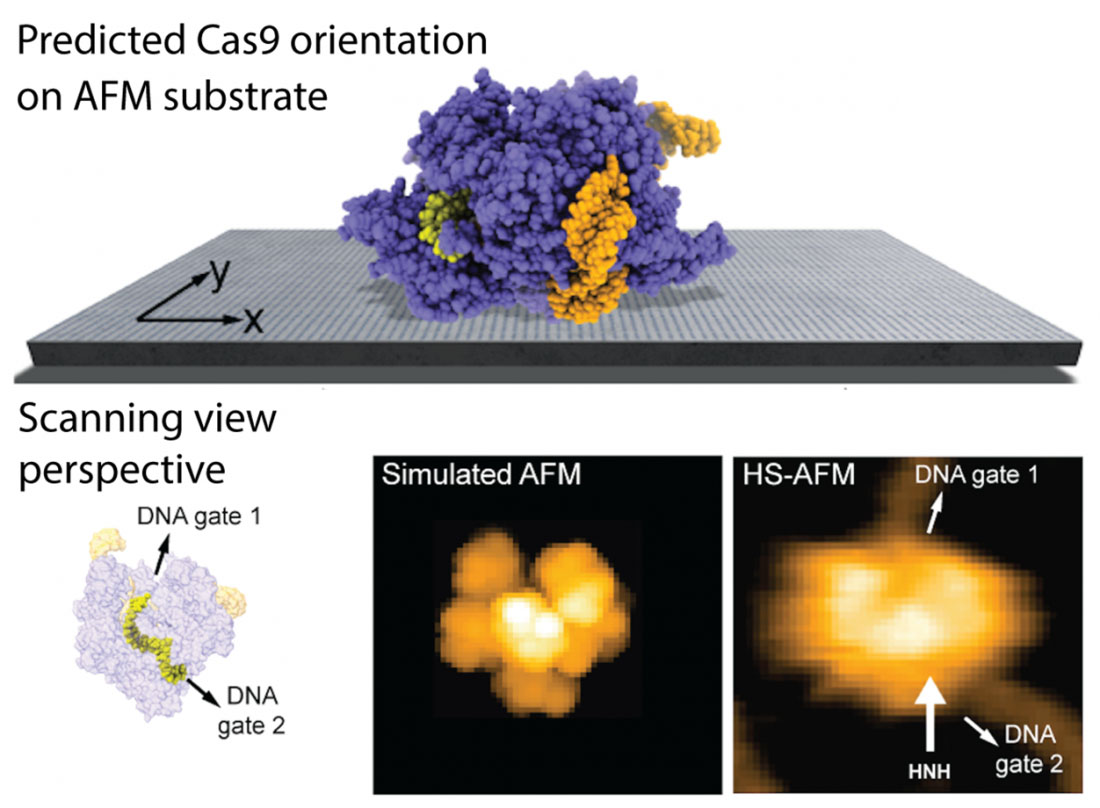
Los autores presentan varias aplicaciones del nuevo método y logran una notable concordancia en las predicciones del modelo con imágenes de proteínas experimentales HS-AFM anteriores. Por ejemplo, los resultados pueden explicar por qué las observaciones HS-AFM de la endonucleasa Cas9, una proteína que desempeña un papel clave en aplicaciones de ingeniería genética, pueden visualizar de manera confiable los movimientos relativos funcionales del ADN objetivo y Cas9 y capturar eventos de escisión del ADN a nivel de una sola molécula. ver figura 1). Además, como se muestra para la máquina chaperona ClpB impulsada por ATP, el modelo puede explicar cómo las condiciones del buffer afectan la estabilidad del complejo muestra-sustrato y validar observaciones de experimentos HS-AFM anteriores.
En resumen, el nuevo método permite utilizar la enorme cantidad de datos estructurales disponibles de biomoléculas para hacer predicciones sobre la colocación de muestras en sustratos de AFM incluso antes de un experimento real, y también se puede utilizar para el análisis post-experimental de AFM. se aplican los datos. El método desarrollado se implementa en el paquete de software BioAFMviewer, disponible de forma gratuita, y proporciona una plataforma práctica para aplicaciones de la amplia comunidad de BioAFM.
[ad_2]

