[ad_1]
(noticias nanowerk) Un equipo de investigación dirigido por el Prof. Jacob Hanna del Instituto Weizmann de Ciencias creó modelos completos de embriones humanos a partir de células madre cultivadas en el laboratorio y logró cultivarlos fuera del útero hasta el día 14. Como se informó en Naturaleza (“Modelos completos de embriones humanos en el día 14 después de la implantación a partir de células ES vírgenes”), estos modelos de embriones sintéticos tenían todas las estructuras y compartimentos característicos de esta etapa, incluida la placenta, el saco vitelino, el saco coriónico y otros tejidos externos que forman Los modelos garantizan un crecimiento dinámico y adecuado.
Los agregados celulares obtenidos de células madre humanas en estudios anteriores no podían considerarse modelos verdaderamente precisos de embriones humanos porque carecían de casi todos los rasgos característicos de un embrión después de la implantación. En particular, no contenían varios tipos de células esenciales para el desarrollo del embrión, como las que forman la placenta y el saco coriónico. Además, no tenían la organización estructural característica del embrión y no mostraban una capacidad dinámica para avanzar a la siguiente etapa de desarrollo.
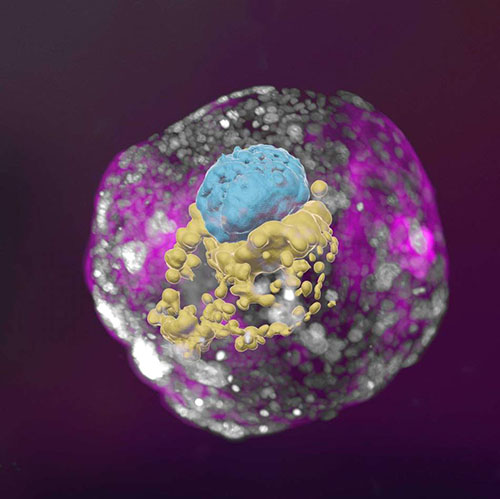
Debido a su auténtica complejidad, los modelos de embriones humanos creados por el grupo de Hanna podrían brindar una oportunidad sin precedentes para arrojar nueva luz sobre los misteriosos orígenes del embrión. Se sabe poco sobre el embrión temprano porque es muy difícil de estudiar por razones éticas y técnicas, pero sus primeras etapas son cruciales para su desarrollo futuro. En estas fases, el conjunto de células que se implanta en el útero al séptimo día de su existencia se convierte, en tres o cuatro semanas, en un embrión bien estructurado que ya contiene todos los órganos del cuerpo.
«El drama tiene lugar en el primer mes, los ocho meses restantes del embarazo son principalmente meses de crecimiento», dice Hanna. “Pero este primer mes sigue siendo en gran medida una caja negra. Nuestro modelo de embrión humano derivado de células madre ofrece una forma ética y accesible de analizar este cuadro. Imita fielmente el desarrollo de un embrión humano real, en particular la formación de su arquitectura extremadamente delicada”.
Deje que el modelo de embrión diga «¡Vamos!»
El equipo de Hanna se basó en su experiencia previa en la creación de modelos de embriones de ratón basados en células madre sintéticas. Como en esta investigación (celúla, “Embriones sintéticos posgastrulación creados ex útero a partir de CME no tratados previamente con ratones”), los científicos no utilizaron óvulos fertilizados ni útero. Más bien, comenzaron con células humanas llamadas células madre pluripotentes, que tienen el potencial de diferenciarse en muchos tipos de células, aunque no en todos. Algunos procedían de células de la piel adulta que se habían convertido nuevamente en «células madre». Otros eran descendientes de líneas de células madre humanas que habían sido cultivadas en el laboratorio durante años.
Luego, los investigadores utilizaron el método desarrollado recientemente por Hanna para reprogramar células madre pluripotentes y retroceder aún más el tiempo: llevar estas células a un estado aún más temprano, el llamado estado ingenuo, en el que son capaces de hacer cualquier cosa, es decir, especializadas. en cada tipo de célula. Esta etapa corresponde al séptimo día del embrión humano natural, aproximadamente en el momento en que se implanta en el útero. De hecho, en 2013, el equipo de Hanna fue el primer equipo en comenzar a describir métodos para generar células madre humanas vírgenes; Han seguido mejorando estos métodos, que forman el núcleo del proyecto actual, a lo largo de los años.
Los científicos dividieron las células en tres grupos. Las células que se convertirían en el embrión se mantuvieron sin cambios. Las células de cada uno de los otros grupos fueron tratadas únicamente con productos químicos, sin necesidad de modificación genética, para activar genes específicos, lo que debería hacer que estas células se diferencien en uno de los tres tipos de tejido necesarios para mantener el embrión: placenta, saco vitelino o la membrana del mesodermo extraembrionario que finalmente forma el saco coriónico.
Poco después de mezclarse en condiciones optimizadas y especialmente diseñadas, las células formaron grupos, aproximadamente el 1 por ciento de los cuales se autoorganizaron en estructuras completas similares a embriones. “Un embrión es, por definición, autodirigido; No necesitamos decirle qué hacer, solo necesitamos desbloquear su potencial codificado internamente”, dice Hanna. “Es crucial mezclar los tipos de células correctos desde el principio, que sólo pueden obtenerse a partir de células madre ingenuas que no estén sujetas a limitaciones de desarrollo. Tan pronto como haces eso, el modelo parecido a un embrión dice: ‘¡Vamos!'».
Las estructuras similares a embriones (SEM, por sus siglas en inglés) basadas en células madre se desarrollaron normalmente fuera del útero durante ocho días, alcanzando una etapa de desarrollo correspondiente al día 14 del desarrollo embrionario humano. En este punto, los embriones naturales adquieren las estructuras internas que les permiten pasar a la siguiente etapa: el desarrollo de los precursores de los órganos del cuerpo.
Los modelos completos de embriones humanos corresponden a diagramas clásicos en términos de estructura e identidad celular.
Cuando los investigadores compararon la organización interna de sus modelos de embriones derivados de células madre con ilustraciones y secciones de anatomía microscópica en atlas de embriología clásicos de la década de 1960, encontraron una asombrosa similitud estructural entre los modelos y los embriones humanos naturales en la etapa correspondiente. Cada compartimento y estructura de soporte no sólo estaba presente, sino también en la ubicación, el tamaño y la forma correctos. Incluso las células que producen la hormona utilizada en las pruebas de embarazo estaban presentes y activas: cuando los científicos introdujeron secreciones de estas células en una prueba de embarazo comercial, el resultado fue positivo.
Esto implicó que sus modelos imitan fielmente el proceso por el cual un embrión temprano adquiere todas las estructuras que necesita para comenzar su transformación en feto. «Muchas pérdidas de embarazos ocurren en las primeras semanas, a menudo antes de que la mujer sepa que está embarazada», dice Hanna. «Aquí es también donde surgen muchos defectos congénitos, aunque normalmente sólo se descubren mucho más tarde». Nuestros modelos pueden utilizarse para descubrir las señales bioquímicas y mecánicas que garantizan un desarrollo adecuado en esta etapa temprana y para mostrar cómo este desarrollo puede salir mal. »
De hecho, el estudio ya ha producido un resultado que puede abrir una nueva dirección para la investigación sobre el fracaso temprano del embarazo. Los investigadores descubrieron que si el embrión no está adecuadamente envuelto por células formadoras de placenta en el tercer día del protocolo (equivalente al décimo día de desarrollo embrionario natural), sus estructuras internas, como el saco vitelino, no se desarrollarán adecuadamente.
“Un embrión no es estático. Tiene que tener las células adecuadas en la organización adecuada y poder seguir desarrollándose: se trata de ser y llegar a ser”, afirma Hanna. «Nuestros modelos completos de embriones ayudarán a los investigadores a responder las preguntas más fundamentales sobre qué determina su crecimiento adecuado».
Este enfoque ético para descubrir los secretos de las primeras etapas del desarrollo embrionario podría abrir numerosas vías de investigación. Podría ayudar a descubrir las causas de muchos defectos congénitos y tipos de infertilidad. También podría conducir a nuevas tecnologías para el cultivo de tejidos y órganos para trasplantes. Y podría proporcionar una forma de evitar experimentos que no se pueden realizar con embriones vivos; por ejemplo, determinar los efectos de la exposición a drogas u otras sustancias en el desarrollo fetal.
[ad_2]

