[ad_1]
(noticias nanowerk) Los investigadores llevan mucho tiempo intentando desarrollar herramientas versátiles que permitan la manipulación e identificación precisas del ADN y otras nanopartículas biológicas. Las pinzas ópticas, que utilizan láseres para capturar partículas pequeñas, proporcionan control sin contacto pero no pueden detectar secuencias de ADN específicas.
Al mismo tiempo, la edición de genes CRISPR se ha convertido en un método de detección extremadamente sensible, pero requiere mejoras e integración con la nanotecnología. Ahora, investigadores de la Universidad de Shenzhen y la Universidad China de Hong Kong han combinado CRISPR con pinzas optotérmicas en una innovación que supera las limitaciones anteriores.
En un nuevo estudio publicado en Luz: ciencia y aplicaciones (“Nanopinzas optotérmicas impulsadas por CRISPR: manipulación diversa de bionanopartículas e identificación de un solo nucleótido”), el equipo presenta las nanopinzas optotérmicas impulsadas por CRISPR (CRONT), una plataforma que permite la captura e identificación simultáneas de ADN con alta precisión. Este avance allana el camino para avances en las pruebas en el lugar de atención, la biodetección y la investigación biofísica fundamental.
Las pinzas ópticas se han convertido en una técnica invaluable desde su invención en 1986, proporcionando un control espaciotemporal sin precedentes sobre partículas microscópicas. Sin embargo, dependen de la transmisión de pulsos de un láser de alta potencia y altamente enfocado, lo que limita la cantidad de materiales que pueden capturarse y plantea el riesgo de fotodaños por el calentamiento local.
Las pinzas optotérmicas se introdujeron hace 15 años como una alternativa prometedora con intensidades significativamente más bajas. Utilizan gradientes de temperatura a microescala y flujos de fluidos cerca de una superficie iluminada que absorbe la luz para manipular partículas a través de difusión térmica y fuerzas convectivas. Sin embargo, hasta la fecha, tanto las pinzas ópticas tradicionales como las técnicas optotérmicas no han podido identificar directamente partículas biológicas mediante señales ópticas. Esta capacidad sólo se ha logrado mediante engorrosos métodos de etiquetado fluorescente.
Paralelamente, el diagnóstico CRISPR ha surgido como un enfoque innovador para detectar secuencias de ácido nucleico con extrema especificidad hasta pares de bases individuales. Sin embargo, la implementación de pruebas de laboratorio en dispositivos de punto de atención sigue siendo un desafío debido a la extensa preparación de muestras y la amplificación del objetivo requeridas. El equipo de Shenzhen-CUHK reconoció el enorme potencial de combinar la detección CRISPR con la manipulación precisa de pinzas optotérmicas en una sola plataforma.
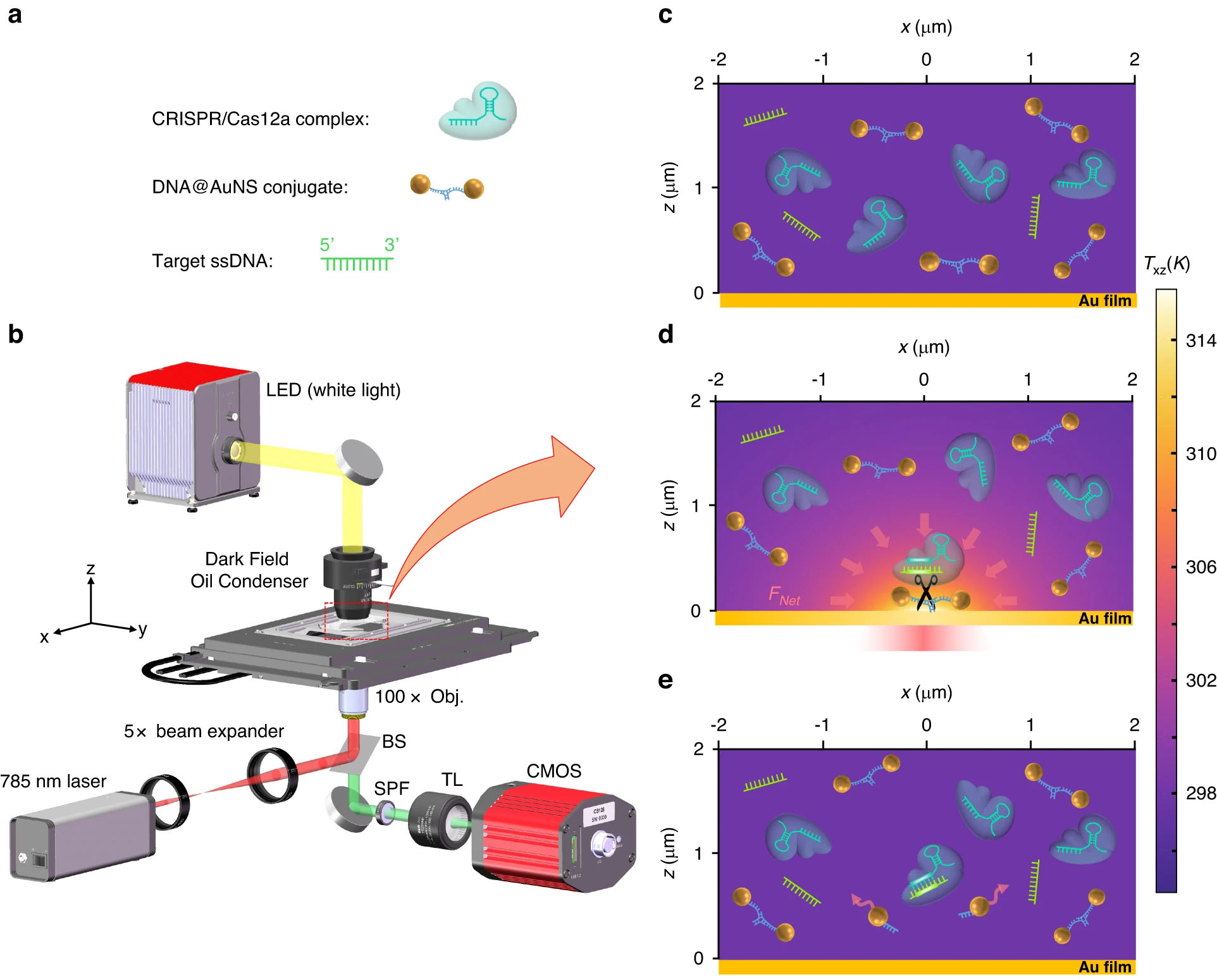
El sistema CRONT utiliza una fina película dorada para producir puntos calientes justo por encima de la temperatura ambiente cuando se ilumina con un puntero láser estándar de 785 nm. Esto crea corrientes de convección localizadas y difusión térmica que pueden capturar selectivamente más de 50 secuencias de ADN diferentes y nanopartículas funcionalizadas con ADN. Una vez capturadas, las secuencias se identifican in situ mediante la introducción de complejos CRISPR que escinden las cadenas de ADN objetivo. Se observa en tiempo real cómo cambia el patrón de difracción de las nanopartículas de oro individuales durante la fragmentación. Esta lectura óptica pasiva evita engorrosos pasos de etiquetado de fluorescencia.
En particular, al aprovechar estas fuerzas de autoensamblaje e integrar sondas CRISPR en los flujos microscópicos inducidos térmicamente, las pinzas CRONT aumentan la concentración y las tasas de interacción para permitir una detección rápida de ADN individual. El equipo demostró sensibilidad attomolar para una secuencia del virus de la viruela simica, sin ninguna amplificación objetivo. Esto representa una mejora de hasta 10 mil millones de veces con respecto a los ensayos CRISPR tradicionales y es equivalente al rendimiento a nivel de PCR. Esta cuantificación altamente sensible en un sistema de pinzas láser de bajo costo podría permitir realizar pruebas en el lugar de atención.
Igualmente notable es que las pinzas CRONT facilitan la detección de polimorfismos de un solo nucleótido (SNP), una capacidad previamente reservada para costosas plataformas de secuenciación o PCR. Esto abre oportunidades para realizar perfiles ópticos de variabilidad genética y mutaciones in situ para estudiar la biodiversidad o los mecanismos de enfermedades. Las validaciones experimentales mostraron que CRONT podía distinguir diferencias de base única entre las variantes del SARS-CoV-2.
Más allá de los ácidos nucleicos, los investigadores demostraron la manipulación programable de proteínas, lo que abre perspectivas interesantes para estudiar las interacciones entre proteínas inducidas por el calor. Y señalan que la plataforma se puede ampliar a diferentes materiales mediante la funcionalización con diferentes sondas.
Si bien siguen siendo una prueba de concepto, las pinzas CRONT, al combinar las ventajas de los ensayos CRISPR y la manipulación optotérmica, superan obstáculos clave que obstaculizan ambas tecnologías de forma independiente. El equipo cree que esto representa un paso importante hacia los biosensores en el punto de atención, la detección de enfermedades, la manipulación celular remota y la integración de la nanofotónica con interacciones biológicas programables. Planean aumentar aún más el rendimiento para acelerar la investigación y el descubrimiento en genómica, epigenética y diagnóstico.
Si se puede mantener la sensibilidad y la simplicidad a medida que avanza la tecnología, las pinzas optotérmicas impulsadas por CRISPR podrían convertirse en una herramienta omnipresente para análisis clínicos y de laboratorio, llevando la nanotecnología avanzada a la biomedicina del mundo real.
[ad_2]

