[ad_1]
(noticias nanowerk) Las modernas técnicas de microscopía permiten examinar el funcionamiento interno de las células con sorprendente detalle. «Ahora podemos observar la disposición y la interacción de proteínas individuales bajo el microscopio», dice el profesor Ralf Jungmann, catedrático de Física Molecular de la Vida en la LMU y becario Max Planck del MPI de Bioquímica.
El equipo del biofísico desarrolló recientemente el revolucionario método RESI (Resolution Enhancement by Sequential Imaging). Con esta técnica, la resolución de la microscopía de fluorescencia se puede mejorar hasta el rango de angstrom, muy por debajo del límite clásico de difracción de la luz. Para ello son cruciales las moléculas marcadoras conjugadas con ADN, que los investigadores unen específicamente a las moléculas que quieren comprender mejor.
El equipo de Jungmann ha presentado una tecnología en la revista especializada Métodos naturales (“Cuantificación de la eficiencia absoluta del etiquetado a nivel de proteína única”), que se puede utilizar para cuantificar qué tan bien se unen las moléculas de biomarcadores a las proteínas diana.
«Esto es absolutamente crucial si se quieren hacer afirmaciones cuantitativamente fiables», explica el físico. Si conoce la eficiencia del etiquetado, puede realizar proteómica resuelta espacialmente de esta manera. Esto permite descubrir no sólo qué hacen las proteínas individuales en una célula, sino también en qué medida están presentes y cómo cambian su cantidad y comportamiento en determinadas circunstancias.
«Pero esto sólo es posible si podemos evaluar qué tan bien funcionó el etiquetado». Porque sólo las proteínas marcadas emiten destellos de luz bajo el microscopio y, por lo tanto, se vuelven visibles.
Fiable y versátil
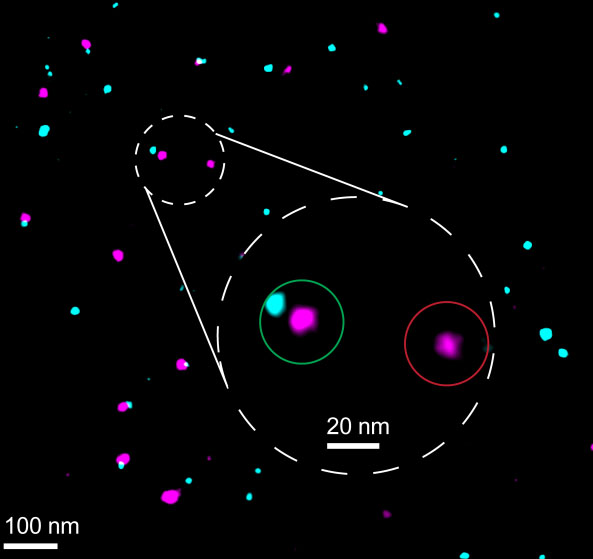
El método desarrollado por el equipo de Jungmann permite esta evaluación añadiendo un biomarcador de referencia a las proteínas diana. Este marcador «brilla» en un color diferente bajo microscopía, por lo que las proteínas marcadas con éxito aparecen en dos colores. El equipo de Jungmann lo demostró utilizando, entre otras cosas, la proteína de membrana CD86: la referencia produce una fluorescencia rosada, el marcador real una azulada. Esto crea un patrón de innumerables puntos de luz rosas y azules. Cuando la marca no funcionó, solo se ilumina el mensaje individualmente. La eficiencia del etiquetado se calcula a partir de la proporción de moléculas doblemente iluminadas y una vez iluminadas.
El método ofrece varias ventajas sobre los métodos anteriores para determinar la eficiencia de unión: «No sólo funciona in vitro, sino también». en vivo“Es decir, en el contexto de células intactas”, explica Jungmann. «La técnica también se puede aplicar a una variedad de objetivos, biomarcadores y muestras diferentes y es compatible con una amplia gama de métodos de alta resolución».
Un medio confiable y generalmente aplicable para evaluar la eficiencia de los marcadores es fundamental para garantizar una interpretación precisa de los datos y permitir comparaciones confiables entre diferentes aglutinantes, condiciones de etiquetado y laboratorios de investigación.
Los autores del estudio están seguros de que el nuevo método de cuantificación ha allanado el camino para ampliar significativamente el potencial de su método microscópico de alta resolución: “Ahora también podemos considerar aplicaciones biomédicas específicas donde la detección cuantitativa de proteínas y procesos es de gran importancia. «Significado», dice Jungmann.
Esto incluye, por ejemplo, la investigación del cáncer, donde la información sobre las interacciones entre las proteínas de la superficie celular y los fármacos a resolución molecular es esencial para el desarrollo de nuevos fármacos.
[ad_2]

