[ad_1]
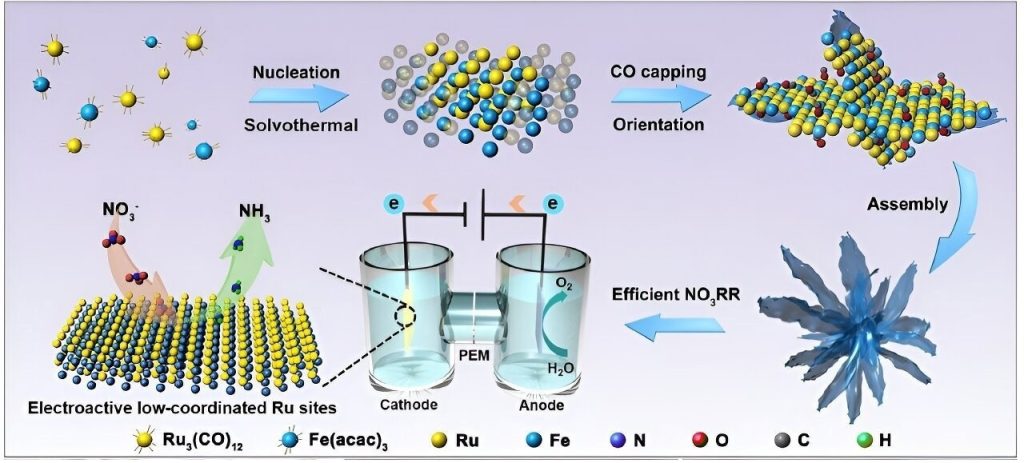
Aunque el amoníaco (NH3) se considera una fuente de energía viable libre de CO2, los expertos de todo el mundo todavía están desconcertados sobre el método de fabricación que consume mucha energía. Para la producción de amoniaco a partir de nitrato (NO).3-), un equipo de investigación dirigido por la Universidad de la Ciudad de Hong Kong (CityU) desarrolló recientemente una aleación bimetálica como nanocatalizador ultrafino que puede ofrecer un rendimiento electroquímico significativamente mejorado. Esto ofrece un gran potencial para la futura producción de combustible neutro en CO2.
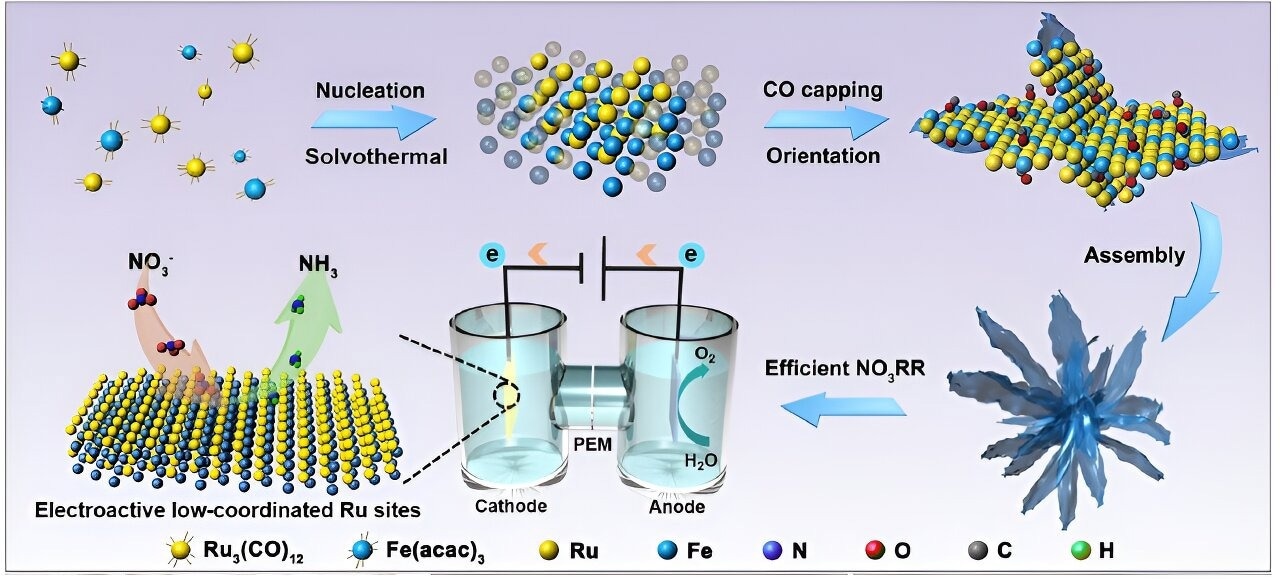
Los resultados, titulados «Ingeniería ambiental de coordinación atómica de nanoestructuras de aleaciones bimetálicas para una electrosíntesis eficiente de amoníaco a partir de nitrato», se publicaron en procedimientos de la Academia Nacional de Ciencias Revista (PNAS).
Debido a que el amoníaco es más fácil de licuar y transportar que el hidrógeno y puede servir como fuente de hidrógeno para pilas de combustible, este ingrediente fertilizante de uso común ha atraído mucho interés recientemente. Reciclaje de nitrato (NO3-) a partir de aguas residuales contaminadas con fertilizantes amónicos se ha convertido en una alternativa viable para producir amoníaco útil y mejorar la sostenibilidad de la agricultura debido a su alta demanda.
Actualmente la reacción electroquímica de reducción de nitrato (NO3RR) se considera un método viable para producir amoníaco. Los electrocatalizadores a base de metales suelen consistir en etapas de desoxigenación e hidrogenación (NO).3– + 9H+ + 8e– ➙ NH3 + 3H2O).
Sin embargo, los subproductos indeseables y la reacción competitiva de evolución de hidrógeno (HER) durante el NO3Aparentemente, la RR dificulta el rendimiento de la producción de amoníaco.
Zhanxi Fan, Director de Estudios y Profesor, Departamento de Química, Universidad de la Ciudad de Hong Kong
A diferencia de estudios anteriores que cambiaron el tamaño o las dimensiones de los electrocatalizadores, el grupo del profesor Fan se centró en mejorar los sitios activos, que son los puntos en la superficie del electrocatalizador donde se unen las moléculas del sustrato y se produce la catálisis.
El fan añadió: “El rutenio (Ru) es un material emergente como electrocatalizador de NO3RR, pero también tiene el problema de favorecer a HER, lo que da como resultado que sus sitios activos estén muy poblados con hidrógeno activo no deseado y no dejen suficiente espacio para la reducción de nitrato a amoníaco.«
Los investigadores añadieron hierro (Fe) para modificar el entorno de coordinación atómica de los sitios activos, sorteando las dificultades. Las estructuras electrónicas y las propiedades superficiales del Ru, y por tanto su actividad catalítica para la producción de amoníaco, se ajustan modificando el entorno de coordinación de los centros de Ru.
El grupo creó nanoflores RuFe, nanohojas ultrafinas dispuestas en forma de flor, utilizando un método de síntesis en un solo recipiente para mejorar aún más la eficiencia del electrocatalizador.
Además de suprimir el HER competitivo y reducir las barreras energéticas al NO3RR, los orbitales complementarios de este catalizador de aleación bimetálica único logran fuertes estados de valencia y una estructura electrónica altamente estable.
Además, los sitios de superficie electroquímicamente activos de las nanoflores de RuFe midieron 267,5 cm2que es mucho más grande que los 105 cm de las nanohojas Ru2 necesarios para que se produzcan las reacciones.
El rendimiento electroquímico de las nanoflores de RuFe mejoró significativamente, como lo demuestra su excepcional eficiencia de Faraday (FE) del 92,9 % y un rendimiento de 38,68 mg h.−1 mgcat−1 para la producción de amoníaco a −0,30 y −0,65 V. Este rendimiento es casi 6,9 veces mayor que el de las nanohojas de Ru puro.
Fan concluyó: “Esta investigación indica un gran potencial para las nanoflores de RuFe en sistemas de energía electroquímica de próxima generación. Creemos que este trabajo puede estimular estudios de seguimiento sobre la modulación del entorno de coordinación atómica de los sitios activos en catalizadores a base de metales para la producción de amoníaco, promoviendo así aún más un ciclo sostenible del nitrógeno para lograr energía libre de carbono en el futuro.«
Referencia de la revista:
Wang, Y, et. Alabama. (2023) Ingeniería del entorno de coordinación atómica de nanoestructuras de aleaciones bimetálicas para una electrosíntesis eficiente de amoníaco a partir de nitrato. procedimientos de la Academia Nacional de Ciencias. doi:10.1073/pnas.2306461120
Fuente: https://www.cityu.edu.hk/
[ad_2]