[ad_1]
(noticias nanowerk) Si las bacterias se dejan solas en nuestros dientes o en la piel lesionada, pueden recubrirse con una estructura viscosa y formar así la llamada biopelícula. Estas bacterias causan estragos en nuestros tejidos y son difíciles de eliminar porque la mucosidad las protege de los antibióticos. Una nueva estrategia puede ofrecer una manera fácil de romper la suciedad y destruir las bacterias.
Investigadores de la Universidad de Pensilvania y la Universidad de Stanford desarrollaron nanopartículas de oro recubiertas de azúcar que les permitieron obtener imágenes y destruir biopelículas. En un estudio publicado en Revista de investigación clínica (“Las nanopartículas teranósticas de jaula de oro en oro permiten la ablación fototérmica y la obtención de imágenes fotoacústicas en modelos de infección asociada a biopelículas”), los autores demostraron el potencial diagnóstico y terapéutico de las nanopartículas en los dientes y la piel lesionada de ratas y ratones y eliminaron las biopelículas. en solo un minuto y supera a los antimicrobianos tradicionales.
“Esta plataforma permite destruir biopelículas sin eliminar quirúrgicamente las infecciones, lo que puede ser necesario cuando se usan antibióticos. «Además, este método podría tratar a pacientes alérgicos a los antibióticos o infectados con cepas resistentes a los medicamentos», dijo Luisa Russell, Ph.D., directora del programa de la División de Ciencia y Tecnología Discovery del NIBIB. «El hecho de que este método no contenga antibióticos es una gran ventaja».
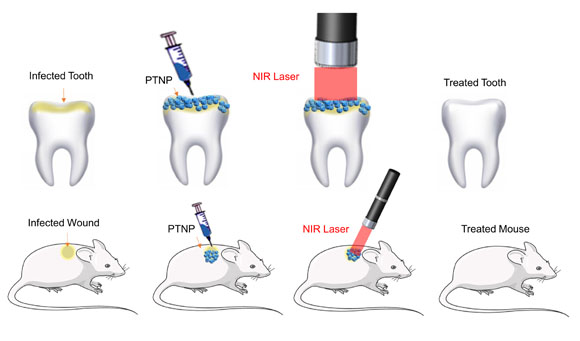
Las biopelículas orales, también llamadas placas, son causadas por bacterias como: estreptococo mutans puede provocar caries importantes. Infecciones de heridas que a menudo son causadas por estafilococos Las bacterias pueden retrasar significativamente el proceso de curación. En ambos casos, la red densa de proteínas y carbohidratos dentro de las biopelículas puede evitar que los antibióticos lleguen a los microbios en toda el área afectada.
Pero ese no es el alcance del problema que plantean las biopelículas. No sólo son difíciles de eliminar, sino que también son difíciles de detectar en primer lugar.
Esta nueva investigación identificó una solución para resolver ambos problemas con una sola piedra: el oro.
El oro no es tóxico y convierte fácilmente la energía de las fuentes de luz en calor, lo que lo convierte en un candidato ideal para la terapia fototérmica, una estrategia que utiliza el calor de las nanopartículas para matar los patógenos cercanos. Además de generar calor, las nanopartículas emiten ondas ultrasónicas detectables en respuesta a la luz, lo que significa que las partículas de oro se pueden visualizar mediante una técnica llamada imágenes fotoacústicas.
En el nuevo estudio, los autores encapsularon esferas de oro dentro de nanopartículas de oro más grandes en forma de jaula para optimizar su respuesta a la luz con fines terapéuticos y de obtención de imágenes. Para hacer que las partículas fueran atractivas para las bacterias, las recubrieron con dextrano, un carbohidrato que es un componente común de las biopelículas.
Los investigadores evaluaron su estrategia depositando nanopartículas de oro sobre ella. S. mutans-dientes infectados por ex-vivo Mandíbula de rata.
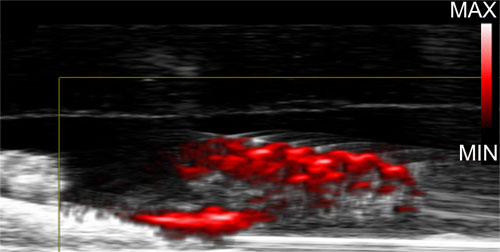
Durante una prueba de imágenes fotoacústicas en los dientes, las nanopartículas emitieron señales fuertes y claras, lo que permitió al equipo ver exactamente dónde las biopelículas habían recogido las partículas recubiertas de dextrano en los dientes.
Luego irradiaron los dientes con un láser para evaluar el efecto terapéutico de las partículas. A modo de comparación, trataron otras muestras de dientes infectados con clorhexidina antiséptica tópica.
El equipo observó un marcado contraste en los resultados de los dos tratamientos: la terapia fototérmica fue casi 100% efectiva para matar biopelículas, mientras que la clorhexidina no afectó significativamente la viabilidad bacteriana.
“El método de tratamiento es especialmente rápido en el caso de las infecciones bucales. Aplicamos el láser durante un minuto, pero en realidad matamos prácticamente todas las bacterias en unos 30 segundos”, dijo la autora principal del estudio, Maryam Hajfathalian, Ph.D., profesora de ingeniería biomédica en el Instituto de Tecnología de Nueva Jersey. quien realizó este estudio como becario postdoctoral en la Universidad de Pensilvania y la Universidad de Stanford.
Los estudios en ratones con heridas abiertas en la piel infectadas con Staphylococcus aureus tuvieron un éxito similar, ya que el calor generado por las nanopartículas superó con creces a otro agente antimicrobiano llamado gentamicina. En este caso, los investigadores también midieron y determinaron un aumento de temperatura de 20 °C localmente en la biopelícula, que aparentemente no causó ningún daño al tejido circundante.
Los autores dicen que quieren utilizar más pruebas para demostrar si la estrategia puede prevenir las caries o acelerar la curación.
“Creo que es importante ver cuán rentable, sencillo y rápido es este proceso. Debido a que tenemos un uso limitado de antibióticos, necesitamos tratamientos novedosos como este para reemplazarlos”, afirmó Hajfathalian.
[ad_2]

